题文
某结晶水合物含有两种阳离子和一种阴离子.称取两份质量均为45.3 g的该结晶水合物,分别制成溶液.向其中一份逐滴加入NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有气体逸出,该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,加热后共计可收集到2.24 L该气体(标准状况);最后白色沉淀逐渐减少并最终消失.另一份逐滴加入Ba(OH)2溶液,开始现象类似,但最终仍有白色沉淀;过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体46.6 g.
请回答以下问题:
(1)该结晶水合物中含有的两种阳离子是________和________,阴离子是________.
(2)该结晶水合物的化__________________________________________________.
(3)假设过程中向该溶液中加入的NaOH溶液的物质的量浓度为5 mol·L-1,请在下图中画出生成沉淀的物质的量与加入NaOH溶液体积的关系示意图.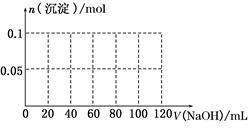
题型:未知 难度:其他题型
答案
】(1) NH4+ 、Al3+ 、SO42-
(2)NH4Al(SO4)2·12H2O[或(NH4)2SO4·Al2(SO4)3·24H2O]
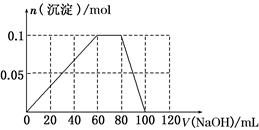
(3)
解析
(1)能使湿润红色石蕊试纸变蓝的气体是NH3,则水合物中有NH4+。加入NaOH溶液,先出现沉淀,后沉淀消失,则水合物中有Al3+.加入Ba(OH)2先出现沉淀,后沉淀溶解,溶解不完.没有溶解的沉淀不溶于HNO3说明含SO42-。
(2)n(SO42-)=
=0.2 mol
n(NH4+)=
=0.1 mol
根据离子化合物中阴、阳离子电荷平衡的原理:n(NH4+)+3n(Al3+)=2n(SO42-)可得:
n(Al3+)=
(2×0.2 mol-0.1 mol)=0.1 mol
n(H2O)=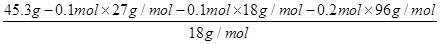
=1.2 mol
该结晶水合物的化学式为NH4 Al(SO4)2·12H2O[或(NH4)2SO4·Al2(SO4)3·24H2O]
(3)Al3+完全沉淀消耗V(NaOH)=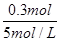
=0.060 L=60 mL
NH4+转化为NH3·H2O消耗V(NaOH)=
=0.020 L=20 mL
Al(OH)3完全溶解消耗V(NaOH)=20 moL。
考点
据考高分专家说,试题“某结晶水合物含有两种阳离子和一种阴离子......”主要考查你对 [物质的量 ]考点的理解。
物质的量
物质的量:
物质中含有一定数目粒子集体的物理量。是国际单位制中7个基本物理量之一(7个基本的物理量分别为:长度、质量、时间、电流强度、发光强度、温度、物质的量)符号:n
计算公式:物质的量(n)=粒子数(N)/阿伏加德罗常数(NA) 以物质的量为中心的各种化学常用量间的关系:n=N/NA=m/M=V/Vm=cV=ρV/M
使用物质的量注意事项:
(1)物质的量表示物质所含指定粒子的多少,物质的量是一个整体,不得简化或增添任何字。
(2)物质的量及其单位摩尔的适用范围是微观粒子,因此在使用中应指明粒子的名称。
物质的量的相关解法:
问题探究:
(1)1mol氢这种说法正确吗?如何表示1mol氢原子、1mol氢分子、1mol氢离子?
答:使用摩尔作单位时,应用化学式(符号)指明离子的种类,1mol氢的说法不正确,因其咩有指明是氢分子还是氢离子、氢原子。1mol氢原子、1mol氢分子、1mol氢离子分别表示为1molH、1molH2、1molH+。
(2)阿佛加德罗常数和6.02×1023mol-1在实际使用上有何区别?
阿佛加德罗常数是一个非常精确的数字,而6.02×1023mol-1只是阿佛加德罗常数的一个近似值。在关于概念性描述时要求非常准确,要使用阿佛加德罗常数,而在涉及计算时,则用6.02×1023mol-1进行粗略计算。二者关系类似于数学上的圆周率∏与3.14的关系。




