题文
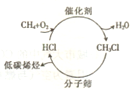
随着石油资源的日趋紧张,天然气资源的转化利用越来越受到人们的关注.如图所示是最近研发出的天然气利用新途径:首先,甲烷在催化剂作用下发生“氧氯化反应”生成一氯甲烷;然后,一氯甲烷在400℃的条件下通过分子筛催化转化为低碳烯烃.
请根据以上信息回答下列问题:
(1)第一轮次反应投料时甲烷和氯化氢的最佳体积比为______.
(2)由一氯甲烷生成丙烯的化学方程式为______.
(3)若该途径中的第一步“甲烷氧氯化反应”的转化率为80%,经除水、分离出混合物中的一氯甲烷后,剩余物质全部留用并投入第二轮次生产;第二步反应生成含有乙烯、丙烯、丁烯的混合气体,碳原子的利用率为90%,分离出其中的烯烃气体后剩余物质全部留用并投入第二轮次生产.则:
①标准状况下,1m3甲烷经过一轮反应可得到______kg乙烯、丙烯、丁烯的混合气体.
②第二轮次反应投料时,需补充的甲烷、氧气和HCl的体积比为______.
题型:未知 难度:其他题型
答案
(1)由信息可知发生的第一步转化为2CH4+2HCl+O2催化剂
2CH3Cl+2H2O,则甲烷和氯化氢的最佳体积比为l:1,故答案为:l:1;(2)一氯甲烷生成丙烯,还应生成HCl,该反应为3CH3Cl分子筛CH2=CH-CH3+3HCl,故答案为:3CH3Cl分子筛CH2=CH-CH3+3HCl;
(3)①由关系式知CH4→(CH2)n,总体转化率为0.9×0.8,标准状况下,1m3甲烷经过一轮反应可得到烯烃的质量为1×0.9×0.822.4×14=0.45kg,故答案为:0.45;
②设初始反应的甲烷量为1,由2CH4+2HCl+O2催化剂2CH3Cl+2H2O、3CH3Cl分子筛CH2=CH-CH3+3HCl,甲烷转化率为80%,则多部反应甲烷剩余0.2,氧气剩余0.1,HCl剩余0.72,一氯甲烷0.08,三者反应的体积比可知需补充甲烷0.8、氧气0.4、氯化氢0.08,最终比例为10:5:1,故答案为:10:5:1.
解析
催化剂
考点
据考高分专家说,试题“随着石油资源的日趋紧张,天然气资源的转化.....”主要考查你对 [化学反应方程式 ]考点的理解。
化学反应方程式
化学方程式:
用化学式来表示化学反应的式子,叫做化学方程式。化学方程式不仅表明了反应物、生成物和反应条件,同时,通过相对分子质量或相对原子质量还可以表示个物质之间的质量关系,即各物质之间的质量比。
书写化学方程式要遵守两个原则:
一是必须以客观事实为基础,绝不能凭空臆想、臆造事实上不存在的物质和化学反应;
二是要遵守质量守恒定律,等号两边各原子种类与数目必须相等。
化学方程式的意义:
化学方程式不仅表明了反应物、生成物和反应条件。同时,化学计量数代表了各反应物、生成物物质的量关系,通过相对分子质量或相对原子质量还可以表示各物质之间的质量关系,即各物质之间的质量比。对于气体反应物、生成物,还可以直接通过化学计量数得出体积比。