题文
(8分)以 ①2NaOH+ Cl2
NaCl+NaClO+H2O ② 2Na + Cl2
2NaCl
③ 2Fe3+ + 2I–
2Fe2+ + I2 ④ 2Fe2+ + Br2
2Fe3+ + 2Br–
这四个反应为例,我们来探究氧化还原反应。
(1)氧化还原反应的本质是 。
(2)对于反应①,氧化剂是 。
(3)对于反应②,Na的化合价由0价变成+1价,化合价升高的原因是 。
(4)由③、④两反应,可以推断Fe3+、Br2、I2的氧化性强弱顺序为 。
题型:未知 难度:其他题型
答案
(1)电子的转移(2)Cl2(3)失去了1个电子(4)Br2 >Fe3+>I2
解析
(1)氧化还原反应的本质是电子的得失或偏移。(2)根据方程式可知,Cl2的化合价降低,所以氧化剂是Cl2。(3))对于反应②,Na的化合价由0价变成+1价,是因为Na失去一个电子,化合价升高。(4)根据氧化剂的氧化性强于氧化产物的氧化性,所以可以推出氧化性Br2 >Fe3+>I2。
点评:本题属于氧化还原反应的基础试题,主要考的是氧化还原的基本概念。
考点
据考高分专家说,试题“(8分)以 ①2NaOH+ Cl2NaC.....”主要考查你对 [氧化还原反应与基本反应类型的关系 ]考点的理解。
氧化还原反应与基本反应类型的关系
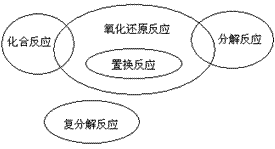
氧化还原反应与基本反应类型的关系:
化合反应有单质参加的是氧化还原反应;分解反应有单质生成的是氧化还原反应;置换反应全部是氧化还原反应;复分解反应都是非氧化还原反应
化学反应的分类:
化学反应按照不同的分类标准,可以分成不同的反应类型
- 根据原子(原子团)的组合形式来分类,把化学反应分为化合反应、分解反应、置换反应、复分解反应,
但是四种基本类型的反应并不能包括所有的化学反应,比如3O2==2O3。 - 按是否有电子转移,把化学反应分为氧化还原反应和非氧化还原反应。
- 按是否有离子参加反应,把化学反应分为离子反应和非离子反应。
- 按化学反应的能量关系,把化学反应分为放热反应和吸热反应。
- ……
null
null
null
null
null