题文
(8分)在K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O反应中, 是氧化剂; 是还原剂; 元素被氧化; 元素被还原; 是氧化产物; 是还原产物;1mol K2Cr2O7反应时转移电子为 mol.
题型:未知 难度:其他题型
答案
(最后一空2分,其余每空1分,共8分)
K2Cr2O7 HCl Cl Cr Cl2 CrCl3 6mol
解析
根据方程式可知,铬元素的化合价从+6价降低到+3价,得到3个电子。氯元素的化合价从-1价升高到0价,失去1个电子。所以K2Cr2O7是氧化剂,HCl是还原剂。Cl元素被氧化,Cr被还原。氯气是氧化产物,CrCl3是还原产物。根据化合价的变化可知,1mol K2Cr2O7反应时转移电子为2mol。
点评:判断氧化还原反应是最关键的是准确判断出有关元素的化合价变化情况,然后根据相应的概念判断即可。而在氧化还原反应的计算中,电子得失守恒是经常用到的关系式。
考点
据考高分专家说,试题“(8分)在K2Cr2O7+14HCl=2.....”主要考查你对 [氧化还原反应与基本反应类型的关系 ]考点的理解。
氧化还原反应与基本反应类型的关系
氧化还原反应与基本反应类型的关系:
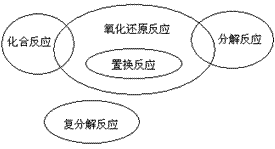
化合反应有单质参加的是氧化还原反应;分解反应有单质生成的是氧化还原反应;置换反应全部是氧化还原反应;复分解反应都是非氧化还原反应
化学反应的分类:
化学反应按照不同的分类标准,可以分成不同的反应类型
- 根据原子(原子团)的组合形式来分类,把化学反应分为化合反应、分解反应、置换反应、复分解反应,
但是四种基本类型的反应并不能包括所有的化学反应,比如3O2==2O3。 - 按是否有电子转移,把化学反应分为氧化还原反应和非氧化还原反应。
- 按是否有离子参加反应,把化学反应分为离子反应和非离子反应。
- 按化学反应的能量关系,把化学反应分为放热反应和吸热反应。
- ……
null
null
null
null
null