题文
常温下KMnO4氧化浓HCl的反应方程式如下:2KMnO4 +16HCl(浓)=2KCl+2MnCl 2+5Cl 2↑+8H2O
(1)用“双线桥法”标明反应中电子转移的方向和数目。
(2)又已知
,结合以上反应原理,则MnO2、KMnO4、Cl2的氧化性由强到弱的顺序是: 。
(3)若有63.2g高锰酸钾参加反应,则被氧化的HCl的物质的量为 mol,产生的Cl2在标准状况下的体积为 L。
题型:未知 难度:其他题型
答案
(1)
(2)KMnO4 MnO2 Cl2 (3)2 22.4
解析
(1)双线桥法标出反应中电子得失数目为
;
(2)2KMnO4 +16HCl(浓)="2KCl" +2MnCl 2+5Cl 2↑ +8H2O此反应制取Cl2不需要条件,而在反应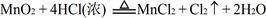
中要加热,且MnO2是氧化剂, Cl2是氧化产物。所以有氧化性KMnO4 >MnO2 >Cl2
(3)高锰酸钾的量、氯气的量以及消耗的盐酸之间的关系为:2KMnO4~5Cl2~16HCl,被氧化的盐酸和参加反应的盐酸的量之比为:10 :16 =5 :8 ,63.2g (即0.4mol)KMnO4完全反应时,产生的Cl2为1.0mol,在标准状况下的体积为1.0mol×22.4L/mol=22.4L,消耗的HCl为3.2mol,被氧化的HCl为2.0mol.
考点
据考高分专家说,试题“常温下KMnO4氧化浓HCl的反应方程式.....”主要考查你对 [氧化还原反应与基本反应类型的关系 ]考点的理解。
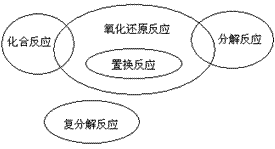
氧化还原反应与基本反应类型的关系
氧化还原反应与基本反应类型的关系:
化合反应有单质参加的是氧化还原反应;分解反应有单质生成的是氧化还原反应;置换反应全部是氧化还原反应;复分解反应都是非氧化还原反应
化学反应的分类:
化学反应按照不同的分类标准,可以分成不同的反应类型
- 根据原子(原子团)的组合形式来分类,把化学反应分为化合反应、分解反应、置换反应、复分解反应,
但是四种基本类型的反应并不能包括所有的化学反应,比如3O2==2O3。 - 按是否有电子转移,把化学反应分为氧化还原反应和非氧化还原反应。
- 按是否有离子参加反应,把化学反应分为离子反应和非离子反应。
- 按化学反应的能量关系,把化学反应分为放热反应和吸热反应。
- ……
null
null
null
null
null