题文
下表为元素周期表的一部分。请回答下列问题:
解析
根据元素在周期表中的相对位置可知①~⑩分别是H、C、N、O、Mg、Al、Cl、Ca、Mn、Fe。
(1)区的名称来自于按照构造原理最后填入电子的轨道名称,所以根据元素的核外电子排布可知,上述元素中,属于s区的是H、Mg、Ca。
(2)氧元素的最外层电子数是6个,所以基态原子的价电子排布图是
或
。
(3)由于Mn元素的3d能级有5个电子,处于半满稳定状态,能量较低,第一电离能大于相邻元素的,所以Mn元素的第一电离能大于铁元素的第一电离能。
(4)根据价层电子对互斥理论可知,氨气分子中氮元素含有的孤对电子对数=(5-3×1)÷2=1,所以氨气的VSEPR模型为四面体;但实际的空间构型是三角锥形,所以该分子为极性分子。由于铜离子能和氨气形成配位健,所以向硫酸铜溶液中逐滴加入其水溶液,可观察到的现象为先产生蓝色沉淀,后溶解得深蓝色溶液。
(5)根据金属铝的晶胞可知,该晶胞的配位数是(3×8)÷2=12个,晶胞含有铝原子的个数是
。根据丙的结构可知,该晶胞的边长是
,所以有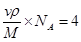
,因此晶胞的密度
g/cm3。
(6)离子晶体的离子半径越小,带电荷数越多,晶格能越大,则晶体的熔沸点越高,则有TiN>MgO,MgO>CaO,由表中数据可知CaO>KCl,因此熔点从高到低的顺序是TiN>MgO>CaO>KCl。氯化钠的配位数是6个,即上下、左右和前后各1各,所以Ca的氧化物晶体中一个阳离子周围和它最邻近且等距离的阳离子有6个。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生能力的培养和解题方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的应试能力和逻辑推理能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力,考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。该题的难点是晶体密度的计算。
考点
据考高分专家说,试题“下表为元素周期表的一部分。请回答下列问题.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




