题文
下图为元素周期表的一部分,根据元素①~⑧在周期表中的位置,按要求回答下列问题。
族
周期
IA
0
1
①
IIA
IIIA
ⅣA
VA
ⅥA
VIIA
2
②
③
3
④
⑤
⑥
⑦
⑧
(1)在元素①~⑧中,金属性最强的元素是_____________(填元素符号),最不容易形成化合物的元素是______________(填元素符号)。
(2)用电子式表示⑦的气态氢化物的形成过程__________________________________。
(3)③、④、⑥中原子半径由大到小的顺序是____________________(填元素符号)。
(4)表中两种元素的原子按1:1组成的常见液态化合物X易被催化分解。某同学取5支大小相同的试管,各加入等物质的量浓度等体积的X溶液,分别进行下列实验,研究外界条件对X分解反应速率的影响,实验记录如下表所示。
序号
条件
现象
结论
温度/℃
催化剂
第一组
1
40
FeCl3溶液
快速产生大量气泡
相同条件下,温度升高,化学反应速率加快
2
20
A
缓慢产生适量气泡
3
5
FeCl3溶液
缓慢产生极少量气泡
第二组
4
t
MnO2
快速产生大量气泡
5
20
无
缓慢产生极少量气泡
①第一组实验目的是:相同条件下,探究________________对该反应速率的影响。
实验2的催化剂A是___________________。
②第二组实验中,实验4的温度t是_________________,发生反应的化学方程式是___________________________________________________________________________。
第二组实验结论是:__________________________________________________。
题型:未知 难度:其他题型
答案
(10分,化学方程式2分,其余每空1分)(1)Na Ar
(2)
解析
根据元素在周期表中的相对位置,元素①~⑧分别是H、O、F、Na、Mg、S、Cl、Ar。
(1)同周期自左向右金属性逐渐降低,同主族自上而下,金属性逐渐升高,所以在元素①~⑧中,金属性最强的元素是Na。最不容易形成化合物的元素是稀有气体元素Ar。
(2)氯元素的气态氢化物是氯化氢,含有共价键的共价化合物,其形成过程可表示为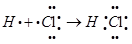
。
(3)同周期自左向右,原子半径逐渐减小,同主族自上而下,原子半径逐渐增大,所以③、④、⑥中原子半径由大到小的顺序是Na>S>F。
(4)①第一组中不同的是温度,因此实验目的是:相同条件下,探究温度对该反应速率的影响。要探究温度对电反应速率对影响,则其它条件都是相同的,因此A是氯化铁溶液。
②第二组实验中中不同的催化剂,因此是探究催化剂对反应速率影响的,因此实验4的温度t仍然是20℃,反应的化学方程式是2H2O2MnO2 2H2O+O2↑。根据实验现象可知,加入催化剂后,能快速的产生大量气泡,所以 结论就是在20℃(或相同条件下),MnO2可以加快H2O2分解的反应速率。
点评:该题是高考中的常见题型,属于基础性的试题。试题基础性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和应试能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力,也有利于培养学生规范严谨的实验设计能力。
考点
据考高分专家说,试题“下图为元素周期表的一部分,根据元素①~⑧.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




