题文
已知A、B、C、D、E是短周期的五种元素,它们的原子序数依次增大。A是短周期元素中原子半径最小的元素;C、D、E三种元素的最高价氧化物对应水化物之间可以两两反应;A与C同主族;B与E同主族;E的单质为淡黄色晶体。
(1)写出E元素在周期表中的位置 ;
(2)写出C元素的离子结构示意图 ;
(3)写出化合物A2B的电子式 ;
(4)写出C、D的最高价氧化物对应水化物相互反应的化学方程式: 。
题型:未知 难度:其他题型
答案
(5分)(1)第三周期第ⅥA族 (2)
解析
A是短周期元素中原子半径最小的元素,则A是氢元素;C、D、E三种元素的最高价氧化物对应水化物之间可以两两反应,则一定含有铝元素,根据原子序数可知D是铝; E的单质为淡黄色晶体,则E是S。B与E同主族,所以B是氧元素。A与C同主族,且C的原子序数大于B的,小于D的,因此C是Na。
(1)E元素在周期表中的位置第三周期第ⅥA族。
(2)C元素的离子结构示意图
。
(3)化合物A2B是水,含有共价键的共价化合物,电子式为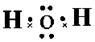
。
(4)氢氧化铝是两性氢氧化物,能溶解在氢氧化钠溶液中,反应的化学方程式是NaOH+Al(OH)3=NaAlO2+2H2O。考点:
点评:该题设计新颖,基础性强,有利于调动学生的学习积极性,激发学生的学习兴趣。该题以“周期表中元素的推断”为载体,比较全面考查学生有关元素推断知识和灵活运用知识的能力。考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。
考点
据考高分专家说,试题“已知A、B、C、D、E是短周期的五种元素.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




