题文
下表为元素周期表的一部分,请参照元素在表中的位置,回答下列问题(凡能用化学用语的必须用相应的化学用语回答):
解析
结合题中周期表可推出:①H ;②C; ③N; ④O ;⑤F ;⑥Na ;⑦Al ;⑧Cl ;⑨Fe ;⑩Br。
(1)中子数为8的N的原子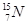
;电子层数等于最外层电子数的元素为H、Al;Cl-有三个电子层,F- 、Na+、Al3+有二个电子层,电子层结构相同,序数越大半径越小。
(2)原子个数比1:2:1形成一种在室内装修过程中常见的气体污染物为甲醛(CH2O), C是SP2杂化;1个CH2O分子中有一个π键,
(3)Na单质在O2中燃烧产生的化合物:Na2O2。
(4)由图中键能数据推断得知结论。
考点
据考高分专家说,试题“下表为元素周期表的一部分,请参照元素在表.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




