题文
己知X、Y、Z、W、N、U、V是短周期的主族元素,原子序数依次增大。X与N同主族,且与W都能形成A2B、A2B2型化合物;Z、W的单质常温下均为无色气体;Y原子的L层电子数是K层电子数的2倍;U原子的最外层电子数是其电子层数的2倍,试回答下列问题:
(1)YW2的电子式 ;Z的氢化物结构式为 ;写出U元素在周期表中的位置 。
(2)原子半径:U V(填>、<或=,下同);气态氢化物的水溶液的酸性:U V。
(3)写出UW2与V元素的单质在水溶液中反应的化学方程式是 。
(4)由X、Z组成的一种化合物化学式为ZX5,其各原子均达到同周期稀有气体原子的稳定结构,该物质属于 (填“离子”或“共价”)化合物。
(5)X、Y、Z、W四种元素(按顺序)可组成原子个数比为5:1:1:3的化合物,该化合物的稀溶液与足量氢氧化钠溶液在加热条件下反应的离子方程式为: 。
题型:未知 难度:其他题型
答案
(1)
;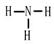
;第三周期第ⅥA族。
(2)>;<。
(3)SO2+Cl2+2H2O=H2SO4+2HCl。
(4)离子。
(5)NH4++HCO3-+2OH-
NH3↑+ CO32-+2H2O。
点击查看构成物质的粒子—分子、原子、离子知识点讲解,巩固学习
解析
根据题意可知这几种元素分别是X:H;Y是C;Z是N;W是O;N是Na;U是S;V是Cl. (1)CO2的电子式为
;Z的氢化物即NH3的结构式为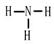
;S是16号元素,核外电子排布为2、8、6,所以Cl元素在周期表中的位置是位于第三周期第ⅥA族。(2)S、Cl是同一周期的元素,由于原子序数Cl>S.原子序数越大,原子的半径就越小。因此原子半径:S>Cl. 气态氢化物的水溶液的酸性H2S是弱酸。HCl是强酸。因此酸性HCl>H2S。(3)SO2有还原性,而Cl2有氧化性,二者在溶液中发生氧化还原反应,方程式为:SO2+Cl2+2H2O=H2SO4+2HCl。(4)由X、Z组成的一种化合物化学式为NH5,其各原子均达到同周期稀有气体原子的稳定结构,该物质结构式为NH4H,属于离子化合物。(5)X、Y、Z、W四种元素(按顺序)可组成原子个数比为5:1:1:3的化合物是NH4HCO3,该化合物是弱酸的酸式盐,其稀溶液与足量氢氧化钠溶液在加热条件下反应的离子方程式为(5)NH4++ HCO3-+ 2OH-
NH3↑+ CO32-+2H2O。
考点
据考高分专家说,试题“己知X、Y、Z、W、N、U、V是短周期的.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




