题文
碳、氮、氧、氟都是位于第二周期的重要的非金属元素。请回答下列问题:
(1)基态氟原子的核外电子排布式是______________ 。
(2)C、N、O、F四种元素第一电离能从大到小的顺序是_________________。
(3)碳和另外三种元素均可形成化合物。四氟化碳的空间构型为____________,CF4可以利用甲烷与Cl2和HF在一定条件下反应来制备,其反应方程式为___________;CO是__________分子(填“极性”或“非极性”),CO的常见等电子体为N2、CN-,已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为___________;C3N4是一种新型材料,它的硬度比金刚石还高,可做切割工具,可推测出C3N4属于_________晶体。
(4)N4分子结构和白磷一样都是正四面体。又已知断裂1molN-N键吸收167kJ热量,生成1 molN≡N键放出942kJ热量,0.1 molN4转变为N2将放出____________热量:
(5)CaF2和CaC2都属于离子晶体。CaF2晶体的密度为a g·cm-3,则晶胞(如图)的体积是_______________(只要求列出算式)。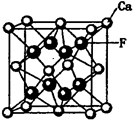
(6)CaC2晶体的晶胞与氯化钠相似,但由于CaC2晶体中的C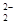
存在,使晶胞沿一个方向拉长,则CaC2晶体中1个C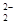
周围距离最近且相等的Ca2+数目为__________,C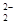
与O
互为等电子体,O
的电子式为____________。
题型:未知 难度:其他题型
答案
(1)1s22s22p5 (1分) (2)F>N>O>C (2分)
(3)正四面体(1分) CH4 + 4 Cl2 + 4 HF 
CF4 + 8 HCl(2分)。
极性(1分) 1:1(或2:2)(1分)原子(1分)
(4) 88.2 kJ(2分) (5)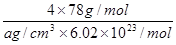
(2分)
(6) 4 (1分)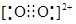
(1分)
点击查看构成物质的粒子—分子、原子、离子知识点讲解,巩固学习
解析
(1)氟是9号元素,基态原子的核外电子排布式是1s22s22p5;
(2) 第一电离能N因2p轨道电子半充满稳定而比O大,故 F>N>O>C;
(3) 四氟化碳的空间构型为正四面体,制备反应是 CH4 + 4 Cl2 + 4 HF 
CF4 + 8 HCl;CO不对称,是极性分子;由N2确定HCN分子的结构式是H—C≡N,分子中σ键与π键数目之比为2:2=1:1;C3N4的硬度比金刚石还高,说明是原子晶体。
(4) N4分子结构和白磷一样都是正四面体,说明有6个N-N。由N4="2" N2可知,0.1 molN4转变为N2将放出热量为0.1×(6×167-2×942)=" 88.2" (kJ)。
(5)晶胞中的Ca2+是4个,F-是8个,由密度为a g·cm-3=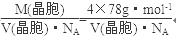
得CaF2晶胞的体积: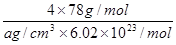
。
(6)CaC2晶体的晶胞与氯化钠相似,Cl-的周围距离最近有6个Na+,由于CaC2晶体中的C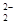
存在,使晶胞沿一个方向拉长,使2Ca2+拉远了,实验CaC2晶体中1个C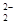
周围距离最近且相等的Ca2+数目为4,C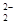
与N2等电子体,故O
与N2等电子体,电子式是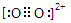
。
考点
据考高分专家说,试题“碳、氮、氧、氟都是位于第二周期的重要的非.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




