题文
(15分)
亚硝酸钠(NaNO2)易溶于水,微溶于乙醚,是常用的食品发色剂
(1)第一电离能:N ___O(填“<”、“>”或“=”);NO2-的空间构型为____
(2)亚硝酸钠在3200C会分解生成氧化钠、一氧化二氮等物质,该反应的化学方程式为____
(3)亚硝酸钠是亚硝酸的钠盐。HNO2的结构如图所示,则HNO2分子中有___个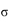
键:
HNO2的酸性比HN03弱是因为_____
(4)亚硝基钻钠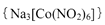
是钴的一种配合物,易溶于水,与钾离子反应生成淡黄色的
沉淀,可用于检验K+的存在。
①基态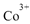
的价层电子排布图为_____
②用亚硝酸钻钠检验K+的离子方程式是
③金属钴的堆积方式如图所示,若一个钴原子的半径为r,,则晶胞的体积V(晶胞)=__
题型:未知 难度:其他题型
答案
(15分)
(1) > (1分) V型或角型(1分)
(2)2NaNO2
Na2O+N2O↑+O2↑(2分)
(3)3(2分)
HNO3中的N的正电性高,导致N—O—H中O的电子向N偏移程度大于HNO3,更容易电离出H+,酸性更强(3分) 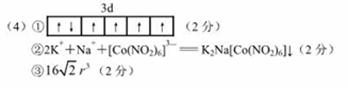
点击查看构成物质的粒子—分子、原子、离子知识点讲解,巩固学习
解析
(1)因为N元素为VA族元素,N原子2p轨道排布3个电子,为半充满状态,为较稳定状态,失去电子较难,所以第一电离能:N > O;NO2-中N价电子为5,所以杂化轨道数=(5+1)÷2=3,所以N原子杂化方式为sp2,所以NO2-的空间构型为V型或角型。
(2)亚硝酸钠在3200C会分解生成氧化钠、一氧化二氮等物质,配平可得化学方程式:2NaNO2
Na2O +N2O↑+O2↑
(3)单键为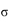
键,双键中的一个键为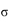
键,根据HNO2的结构简式可知HNO2分子中有3个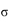
键;HNO3中的N的正电性高,导致N—O—H中O的电子向N偏移程度大于HNO3,更容易电离出H+,酸性更强。
(4)①Co为27号元素,Co3+的价层电子为3d6,所以基态Co3+的3d轨道有1个排布2个电子,其它4个轨道排布1个电子。
②根据亚硝基钻钠{Na3[Co(NO2)6]}与钾离子反应生成淡黄色的K2Na[Co(NO2)6]沉淀,可得离子方程式为:2K++Na++[Co(NO2)6]3- = K2Na[Co(NO2)6]↓
③根据钴晶体堆积方式可知,其晶胞为面向立方,面对角线等于4r,设晶胞的边长为a,则4r=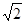
a,可得a=2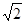
r,则晶胞的体积V(晶胞)=a3=(2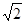
r)3=16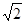
r3。
考点
据考高分专家说,试题“(15分)亚硝酸钠(NaNO2)易溶于水.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




