题文
(15分)开发新型储氢材料是氢能利用的重要研究方向。
(1)化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=NH)3通过如下反应制得:3CH4+2(HB=NH)3+6H2O=3CO2+6H3BNH3。请回答:
①H3BNH3中是否存在配位键 (填“是”或“否”),B、C、N、O第一电离能由大到小的顺序为 ,CH4、H2O、CO2三分子按照键角由大到小的顺序排列为 。
②与(HB=NH)3互为等电子体的分子为 (填分子式)
③人工可以合成硼的一系列氢化物,其物理性质与烷烃相似,故称之为硼烷。工业上可采用LiAlH4和BCl3在一定条件下制备乙硼烷B2H6,该反应的化学方程式为 。
④在硼酸盐中,阴离子有链状、环状、骨架状等多种结构形式。图a为一种无限长链状结构的多硼酸根,其化学式为 ,图b为硼砂晶体中阴离子,其中硼原子采取的杂化方式为 。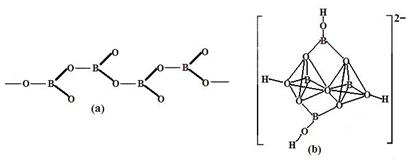
(2)一种铜合金具有储氢功能
①Cu2+的价层电子排布式为 。
②铜及其它许多金属及其化合物都可以发生焰色反应,其原因是 。
③铜的单质中按ABCABC……方式堆积,设铜原子半径为a pm,则该晶体的密度为 g/cm3(阿伏伽德罗常数值为NA)
题型:未知 难度:其他题型
答案
(1)①是,N>O>C>B CO2>CH4>H2O;②C6H6 ;③4BCl3+3LiAlH4=2B2H6+3LiCl+3AlCl3
(或4BCl3+3LiAlH4=2B2H6+3LiAlCl4)④BO2--;sp3、sp2;(2)①3d9;②激发态的电子从能量较高的轨道跃迁到能量较低的轨道时,以一定波长的光的形式释放能量;③
。
点击查看构成物质的粒子—分子、原子、离子知识点讲解,巩固学习
解析
(1)①在H3BNH3中的B与N原子之间存在配位键;B、C、N、O是同一周期的元素。一般情况下,元素的非金属性越强,原子半径越小,元素的第一电离能既有越大,但是由于N原子的2p轨道上的电子处于半充满的稳定状态,所以其电离能比O还大。因此第一电离能由大到小的顺序N>O>C>B;CH4是正四面体结构,键角109°28′;H2O是V型分子,键角104.3°,CO2是直线型分子,键角为180°。因此这三分子按照键角由大到小的顺序排列为CO2>CH4>H2O;②等电子体是原子数等,最外层电子数也相等的物质。与(HB=NH)3互为等电子体的分子为C6H6 ;③根据题意可得合成乙硼烷B2H6,的化学方程式为4BCl3+3LiAlH4=2B2H6+3LiCl+3AlCl3;也可写作4BCl3+3LiAlH4=2B2H6+3LiAlCl4。④多硼酸根的化学式为BO2--;在图b硼原子采取的杂化方式为sp3、sp2;(2)①Cu是29号元素,Cu2+的价层电子排布式为3d9;②铜及其它许多金属及其化合物都可以发生焰色反应的原因是在灼烧时原子中的电子吸收能量,从基态跃迁到激发态。但是激发态是不稳定的,激发态的电子从能量较高的轨道跃迁到能量较低的轨道时,以一定波长的光的形式释放能量;③Cu是面心立方紧密堆积,在一个晶胞中含有的Cu原子的个数为:8×1/8+6×1/2="4;" 设铜原子半径为a pm.晶胞的边长L.
;L=2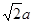
;该晶体的密度为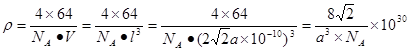
g/cm3.
考点
据考高分专家说,试题“(15分)开发新型储氢材料是氢能利用的重.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




