题文
(9分)元素周期律是指导我们学习元素及其化合物知识的重要工具。已知氧族元素(不含Po)的部分知识如下表所示,
元素
8O
16S
34Se
52Te
单质熔点(℃)
-218.4
113
450
单质沸点(℃)
-183
444.6
685
1390
元素主要化合价
-2
-2,+4,+6
-2,+4,+6
原子半径
逐渐增大
单质与H2反应情况
点燃时易化合
加热化合
加热难化合
不能直接化合
请总结表中知识规律,并依据元素周期律回答下列问题:
(1)单质硒的熔点范围可能是________________。
(2)元素碲的主要化合价可能有________________。
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是________________(用化学式表示)。
(4)氢硒酸有较强的__________(填“氧化性”或“还原性”),因此露置在空气中长期保存易变质,其可能发生反应的化学方程式为_________________________________。
(5)下图所示为氧族元素单质与H2反应过程中的能量变化示意图,其中a、b、c、d分别表示氧族元素中某一元素的单质,纵坐标为相同物质的量的单质与H2反应过程中的能量变化(能量变化>0表示放热,能量变化<0表示吸热)。则:b代表___________ _____, d代表 (均写单质名称)。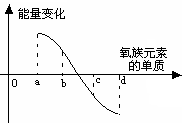
题型:未知 难度:其他题型
答案
(1)大于113℃,小于450℃(1分) (2)-2,+4,+6 (1分)
(3)H2Te>H2Se>H2S (2分) (4)还原性(1分),2H2Se+O2==2Se+2H2O(2分)
(5)硫(1分),碲(1分)。
点击查看构成物质的粒子—分子、原子、离子知识点讲解,巩固学习
解析
(1)根据在氧族元素中单质熔点的变化从8O到52Te逐渐升高的规律中得到。
(2)在同一主族中元素的主要化合价相同故碲的主要化合价可能有-2,+4,+6。
(3)在同一主族中,元素原子序数越大,元素的非金属性越弱,形成的氢化物的稳定性越差,氢化物水溶液的酸性越强,故硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是H2Te>H2Se>H2S。
(4)在同一主族中,形成的简单阴离子的还原性随原子序数增大而增强,故氢硒酸有较强的还原性。
(5)在此反应过程中放出的能量越多氢化物的稳定性越强,得到a的氢化物最稳定,d的氢化物稳定性最差,可得。
考点
据考高分专家说,试题“(9分)元素周期律是指导我们学习元素及其.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




