题文
将一定质量的Mg-A1合金投入100mL一定物质的量浓度的某HCl溶液中,充分反应.向反应后的溶液中逐滴加入一定物质的量浓度的NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积关系如右图.计算下列问题:(写出简要计算过程) 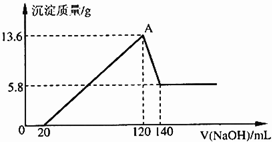
(1)求合金中Mg与Al的物质的量之比?
(2)所加NaOH溶液的物质的量浓度是多少?
(3)原HCl溶液的物质的量浓度是多少?
题型:未知 难度:其他题型
答案
(1)由图象可知溶于NaOH溶液的沉淀为13.6g-5.8g=7.8g,该沉淀为Al(OH)3,
物质的量为n(Al(OH)3)=7.8g78g/mol=0.1mol,即0.1molAl(OH)3,
不溶于NaOH溶液的Mg(OH)2沉淀为5.8g,物质的量为n(Mg(OH)2)=5.8g58g/mol=0.1mol,
原合金中n(Al)=n(Mg)=0.1mol,故物质的量之比是1:1.
答:合金中Mg与Al的物质的量之比为1:1.
(2)由Al(OH)3与NaOH反应的方程式计算,
Al(OH)3+OH-═AlO2-+H2O
1mol 1mol
0.1mol c(NaOH)×(140-120)×10-3
得c(NaOH)=5mol•L-1
答:所加NaOH溶液的物质的量浓度是5mol•L-1.
(3)图象中A点为沉淀量最大时,此时溶液溶质为NaCl,故n(Na+)=n(Cl-)=0.12L×5mol•L-1=0.6mol,
c(HCl)=0.6mol0.1L=6mol•L-1
答:原HCl溶液的物质的量浓度是6mol•L-1.
解析
7.8g78g/mol
考点
据考高分专家说,试题“将一定质量的Mg-A1合金投入100mL.....”主要考查你对 [物质的量浓度 ]考点的理解。
物质的量浓度
物质的量浓度:
定义:单位体积的溶液里所含溶质B的物质的量,也称为B的物质的量浓度
符号:cB
单位:mol/L(mol·L -1)
计算公式:物质的量浓度(cB)=物质的量(n)/溶液的体积(V)
物质的量浓度与溶液质量分数、密度的关系:c=1000ρω/M
稀释定理:
- 稀释前后溶液中溶质的物质的量不变
c(浓溶液)V(浓溶液)=c(稀溶液)V(稀溶液) - 稀释前后溶液中溶质的质量不变
ρ(浓溶液)V(浓溶液)w%(浓溶液)=ρ(稀溶液)V(稀溶液)w%(稀溶液)
null
null
物质的量浓度与质量分数(质量百分比浓度)的比较:
浓度计算的注意事项:
物质的量浓度(cB)=物质的量(n)/溶液的体积(V)
(1)V指溶液体积而不是溶剂的体积;
(2)取出任意体积的1mol/L溶液,其浓度都是1mol/L。但所含溶质的量则因体积不同而不同;
(3)“溶质”是溶液中的溶质,可以是化合物,也可以是离子或气体特定组合,特别的,像NH3、Cl2等物质溶于水后成分复杂,但求算浓度时,仍以溶解前的NH3、Cl2为溶质,如氨水在计算中使用摩尔质量时,用17g/mol。
溶液中溶质的质量分数与溶质的物质的量浓度的换算:
- 溶液中溶质的质量可以用溶质的质量分数表示: m(溶质)=ρ(g·cm-3)·V(L)·w% (1cm3=1mL)
- 溶液中溶质的质量可以用物质的量浓度来表示: m(溶质)=c(mol/L)·V(L)·M(g·mol-1)
- 由于同一溶液中溶质的质量相等,溶液的体积也相等,但注意:1L=1000mL,所以,上述两式可以联系起来:
ρ(g·cm-3)·1000V(mL)·w%=c(mol/L)·V(L)·M(g·mol-1) 化简得:1000ρw%=cM
null
null
null




