题文
为了测定某种烷烃(不溶于水,密度比空气大)样品的平均相对分子质量,设计了下面的实验:
①取一个配有合适胶塞的洁净、干燥的锥形瓶,准确称其质量为m1;
②往锥形瓶中通入干燥的该烃的样品,塞好胶塞,准确称量,重复操作,直到前后两次称量结果基本相同,得到质量为m2;
③往锥形瓶中加满水,塞好胶塞,准确称量,得到质量为m3。已知:空气的平均相对分子质量为29.0,完成下列问题: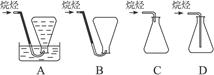
可供选用的装置
(1)具体说明本实验的原理________________________________________________。
(2)步骤②为什么要重复操作直到前后两次称量的结果基本相同?___________________。
(3)具体说明本实验中如何做到每次测量都在相同体积下进行________________________。
(4)本实验中收集气体样品的操作,可选用的方法是(用图中的标号填写)_____________。
(5)写出锥形瓶中样品的质量m样品的计算式____________________(设空气的质量为m空气)
(6)写出由实验测得该烷烃的平均相对分子质量为____________________(计算式)。
题型:未知 难度:其他题型
答案
(1)根据阿伏加德罗定律——同温、同压下,同体积的两种不同气体的质量之比等于相对分子质量之比
(2)保证瓶内空气完全排尽,样品恒重
(3)在第一次称量前,待锥形瓶塞紧胶塞后,在瓶口胶塞上做一标记,以后每次测量,胶塞塞入瓶口的位置都以此为准
(4)D
(5)m2-m1+m空气
(6)29.0×
或29.0×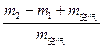
解析
测定烷烃样品的平均相对分子质量用的是阿伏加德罗定律的推论,即
;在测量过程中采用了测平均数据法(重复操作、两次测量结果基本相同)可保证实验时瓶内空气完全排尽,使结果准确;为使每次测量都在相同的体积下进行,便须对锥形瓶中所容纳物质的体积进行标记;由于空气的平均相对分子质量为29.0,而样品的平均相对分子质量大于29.0,故要采用向上排空气法收集(注意不能用排水法,否则将在样品中混入水蒸气而影响测定结果);由实验操作可知,m1为锥形瓶与空气的总质量,m2为锥形瓶与烷烃样品的总质量,则m样品=m2-m1+m空气。
考点
据考高分专家说,试题“为了测定某种烷烃(不溶于水,密度比空气大.....”主要考查你对 [物质的量 ]考点的理解。
物质的量
物质的量:
物质中含有一定数目粒子集体的物理量。是国际单位制中7个基本物理量之一(7个基本的物理量分别为:长度、质量、时间、电流强度、发光强度、温度、物质的量)符号:n
计算公式:物质的量(n)=粒子数(N)/阿伏加德罗常数(NA) 以物质的量为中心的各种化学常用量间的关系:n=N/NA=m/M=V/Vm=cV=ρV/M
使用物质的量注意事项:
(1)物质的量表示物质所含指定粒子的多少,物质的量是一个整体,不得简化或增添任何字。
(2)物质的量及其单位摩尔的适用范围是微观粒子,因此在使用中应指明粒子的名称。
物质的量的相关解法:
问题探究:
(1)1mol氢这种说法正确吗?如何表示1mol氢原子、1mol氢分子、1mol氢离子?
答:使用摩尔作单位时,应用化学式(符号)指明离子的种类,1mol氢的说法不正确,因其咩有指明是氢分子还是氢离子、氢原子。1mol氢原子、1mol氢分子、1mol氢离子分别表示为1molH、1molH2、1molH+。
(2)阿佛加德罗常数和6.02×1023mol-1在实际使用上有何区别?
阿佛加德罗常数是一个非常精确的数字,而6.02×1023mol-1只是阿佛加德罗常数的一个近似值。在关于概念性描述时要求非常准确,要使用阿佛加德罗常数,而在涉及计算时,则用6.02×1023mol-1进行粗略计算。二者关系类似于数学上的圆周率∏与3.14的关系。




