题文
取不同质量的镁铝合金分别与25 mL同浓度的稀硝酸反应,测量合金的质量与产生气体的体积(标准状况),列表如下:
实验编号
合金质量(mg)
气体体积(mL)
1
144
112
2
288
224
3
864
560
若第3个实验后向反应容器内加入足量的1.0 mol/L NaOH(aq)充分反应,使固体质量不再发生变化。硝酸的浓度及至少需要NaOH(aq)的体积是
硝酸的浓度
NaOH(aq)的体积
A.
B.
C.
D.
4.0 mol/L
1.0 mol/L
75 mL
99 mL
题型:未知 难度:其他题型
答案
AD
解析
分析1、2组数据可知,金属的质量之比等于对应NO的体积之比,说明1、2组金属完全反应,第3组金属若完全反应,可得NO体积为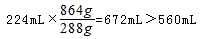
,故第3组金属有剩余,硝酸完全反应。第3个实验后向反应容器内加入足量的1.0mol/L NaOH(aq)充分反应,使固体质量不再发生变化,使氢氧化铝恰好转化为NaAlO2,需要氢氧化钠溶液的体积最小,此时溶液中溶质为NaNO3、NaAlO2,第3组生成的NO的物质的量为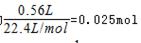
,由反应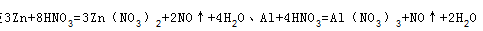
可知,起氧化剂作用的硝酸为总的硝酸的1 4 ,故25mL硝酸溶液中
=0.1mol,原硝酸溶液的浓度为
。起酸性作用的硝酸的物质的量为0.1mol-0.025mol=0.075mol,
令144mg合金中Mg、Al的物质的量分别为xmol、ymol,由二者质量与转移电子数目守恒有:
解得x=0.0015,y=0.004,故864mg合金中Al的物质的量 
,根据钠离子守恒可知n(NaOH)=n(NaNO3)+n(NaAlO2)=0.075mol+0.024mol=0.099mol,故需要氢氧化钠溶液的最小体积为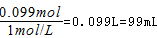
,故选AD。
考点
据考高分专家说,试题“取不同质量的镁铝合金分别与25 mL同浓.....”主要考查你对 [物质的量 ]考点的理解。
物质的量
物质的量:
物质中含有一定数目粒子集体的物理量。是国际单位制中7个基本物理量之一(7个基本的物理量分别为:长度、质量、时间、电流强度、发光强度、温度、物质的量)符号:n
计算公式:物质的量(n)=粒子数(N)/阿伏加德罗常数(NA) 以物质的量为中心的各种化学常用量间的关系:n=N/NA=m/M=V/Vm=cV=ρV/M
使用物质的量注意事项:
(1)物质的量表示物质所含指定粒子的多少,物质的量是一个整体,不得简化或增添任何字。
(2)物质的量及其单位摩尔的适用范围是微观粒子,因此在使用中应指明粒子的名称。
物质的量的相关解法:
问题探究:
(1)1mol氢这种说法正确吗?如何表示1mol氢原子、1mol氢分子、1mol氢离子?
答:使用摩尔作单位时,应用化学式(符号)指明离子的种类,1mol氢的说法不正确,因其咩有指明是氢分子还是氢离子、氢原子。1mol氢原子、1mol氢分子、1mol氢离子分别表示为1molH、1molH2、1molH+。
(2)阿佛加德罗常数和6.02×1023mol-1在实际使用上有何区别?
阿佛加德罗常数是一个非常精确的数字,而6.02×1023mol-1只是阿佛加德罗常数的一个近似值。在关于概念性描述时要求非常准确,要使用阿佛加德罗常数,而在涉及计算时,则用6.02×1023mol-1进行粗略计算。二者关系类似于数学上的圆周率∏与3.14的关系。




