题文
WO3可用于制备电阻元件、电子射线屏等。其工业生产流程如下: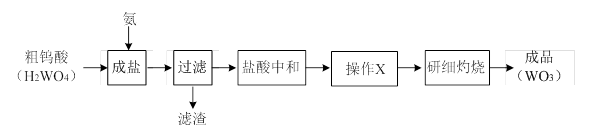
(1)操作X的目的是为了获得纯净的仲钨酸铵晶体,该操作包括:将用盐酸中和后的溶液 、冷却结晶、 、低温烘干。
(2)实际工业生产中,粗仲钨酸铵晶体(含少量NH4Cl晶体)可不经提纯就直接灼烧,其原因是 。
(3)已知:仲钨酸铵晶体[x(NH4)2O·yWO3·zH2O]受热分解的化学方程式如下:
x(NH4)2O·yWO3·zH2O→WO3 +NH3↑+H2O↑(未配平)。
某同学为测定仲钨酸铵晶体的组成,进行如下实验:
①准确称取16.21g样品,研细灼烧;
②将产生的气体通入装有碱石灰干燥管,充分吸收称得干燥管增重1.44g;
③称量冷却后的固体质量为13.92g。
通过计算确定此仲钨酸铵晶体的化学式(写出计算过程)。
题型:未知 难度:其他题型
答案
(1)加热浓缩 过滤、洗涤
(2)杂质NH4Cl被灼烧分解后全部转化为气体
(3)m(NH3)=16.21g-13.92g-1.44g=0.85g
n(NH4+)=n(NH3)=" 0.85g" ÷17g·mol—1=0.05mol
样品中结晶水:n(H2O)="1.44" g ÷18 g·mol—1-0.05mol÷2="0.055" mol
n(WO3)=13.92g÷232 g·mol—1=0.06mol
x:y:z="0.025" mol:0.06mol:0.055 mol=5:12:11
故仲钨酸铵晶体的化学式为5(NH4)2O·12WO3·11H2O。
解析
(1)将溶液蒸发浓缩后才能冷却结晶,晶体与溶液分开采用过滤的方法,并要洗涤除去晶体表面杂质;(2)NH4Cl受热分解为HCl和NH3,从固体中分离;
(3)物质组成的计算
根据②步干燥管增重为水的量
样品中结晶水:n(H2O)="1.44" g ÷18 g·mol—1-0.05mol÷2="0.055" mol
根据质量守恒计算产生氨气的量,计算NH4+的量
m(NH3)=16.21g-13.92g-1.44g=0.85g
n(NH4+)=n(NH3)=" 0.85g" ÷17g·mol—1="0.05mol"
根据③步得到固体为WO3,n(WO3)=13.92g÷232 g·mol—1=0.06mol
所以有x:y:z="0.025" mol:0.06mol:0.055 mol=5:12:11
故仲钨酸铵晶体的化学式为5(NH4)2O·12WO3·11H2O。
考点
据考高分专家说,试题“WO3可用于制备电阻元件、电子射线屏等。.....”主要考查你对 [物质的量 ]考点的理解。
物质的量
物质的量:
物质中含有一定数目粒子集体的物理量。是国际单位制中7个基本物理量之一(7个基本的物理量分别为:长度、质量、时间、电流强度、发光强度、温度、物质的量)符号:n
计算公式:物质的量(n)=粒子数(N)/阿伏加德罗常数(NA) 以物质的量为中心的各种化学常用量间的关系:n=N/NA=m/M=V/Vm=cV=ρV/M
使用物质的量注意事项:
(1)物质的量表示物质所含指定粒子的多少,物质的量是一个整体,不得简化或增添任何字。
(2)物质的量及其单位摩尔的适用范围是微观粒子,因此在使用中应指明粒子的名称。
物质的量的相关解法:
问题探究:
(1)1mol氢这种说法正确吗?如何表示1mol氢原子、1mol氢分子、1mol氢离子?
答:使用摩尔作单位时,应用化学式(符号)指明离子的种类,1mol氢的说法不正确,因其咩有指明是氢分子还是氢离子、氢原子。1mol氢原子、1mol氢分子、1mol氢离子分别表示为1molH、1molH2、1molH+。
(2)阿佛加德罗常数和6.02×1023mol-1在实际使用上有何区别?
阿佛加德罗常数是一个非常精确的数字,而6.02×1023mol-1只是阿佛加德罗常数的一个近似值。在关于概念性描述时要求非常准确,要使用阿佛加德罗常数,而在涉及计算时,则用6.02×1023mol-1进行粗略计算。二者关系类似于数学上的圆周率∏与3.14的关系。




