题文
2012年3月21 日是第二十届“世界水日”,保护水资源,从我做起!
(1)ClO2和Cl2(还原产物都为Cl-)是生活中常用的消毒剂。当消耗等物质的量的两种物质时,ClO2的消毒效率是Cl2的________倍。
(2)某无色废水中可能含有Fe3+、Al3+、Mg2+、Na+、NO3—、CO32—、SO42—离子中的几种,为分析其成分,分别取废水样品100 mL,进行了三组实验,其操作和有关现象如下图所示: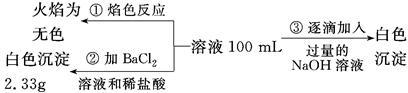

请根据上图回答下列问题:
①实验中需配制1.0 mol/L的NaOH溶液100 mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为_________________________________________。
②实验③中沉淀量由A→B过程中所发生反应的离子方程式为____________________。
③试确定NO3—是否存在?________(填“存在”、“不存在”或“不确定”),若存在,试计算c(NO3—)=________(若不存在,此问不必作答)。
题型:未知 难度:其他题型
答案
(1)2.5 (2)①100mL容量瓶 ②Al(OH)3+OH-=AlO2—+2H2O ③存在 0.15 mol/L
解析
(1)一个 ClO2生成Cl-,得到5个电子,一个Cl2生成2个Cl-,得到2个电子,所以ClO2的消毒效率是Cl2的2.5倍。
(2)①需要100 mL容量瓶;②反应的离子方程式为Al(OH)3+OH-=AlO2—+2H2O;
③无色废水→不含Fe3+;焰色反应无色→不含Na+;向废水中加过量氢氧化钠溶液有白色沉淀生成,且有部分溶解→含有Mg2+、 Al3+;溶液中含有Mg2+、Al3+,一定不含CO32—;白色沉淀BaSO4 2.33 g的物质的量为0.01 mol→SO42—的物质的量也是0.01 mol。
n(NaOH)=n(Al3+)=0.005 mol
n[Mg(OH)2]=n(Mg2+)=0.01 mol
设硝酸根离子的物质的量是X,根据溶液中阴阳离子电荷守恒知。
0.01×2+0.005×3=X+0.01×2 X=0.015 mol
考点
据考高分专家说,试题“2012年3月21 日是第二十届“世界水.....”主要考查你对 [物质的量 ]考点的理解。
物质的量
物质的量:
物质中含有一定数目粒子集体的物理量。是国际单位制中7个基本物理量之一(7个基本的物理量分别为:长度、质量、时间、电流强度、发光强度、温度、物质的量)符号:n
计算公式:物质的量(n)=粒子数(N)/阿伏加德罗常数(NA) 以物质的量为中心的各种化学常用量间的关系:n=N/NA=m/M=V/Vm=cV=ρV/M
使用物质的量注意事项:
(1)物质的量表示物质所含指定粒子的多少,物质的量是一个整体,不得简化或增添任何字。
(2)物质的量及其单位摩尔的适用范围是微观粒子,因此在使用中应指明粒子的名称。
物质的量的相关解法:
问题探究:
(1)1mol氢这种说法正确吗?如何表示1mol氢原子、1mol氢分子、1mol氢离子?
答:使用摩尔作单位时,应用化学式(符号)指明离子的种类,1mol氢的说法不正确,因其咩有指明是氢分子还是氢离子、氢原子。1mol氢原子、1mol氢分子、1mol氢离子分别表示为1molH、1molH2、1molH+。
(2)阿佛加德罗常数和6.02×1023mol-1在实际使用上有何区别?
阿佛加德罗常数是一个非常精确的数字,而6.02×1023mol-1只是阿佛加德罗常数的一个近似值。在关于概念性描述时要求非常准确,要使用阿佛加德罗常数,而在涉及计算时,则用6.02×1023mol-1进行粗略计算。二者关系类似于数学上的圆周率∏与3.14的关系。




