题文
在Cu+2H2SO4(浓) △ . CuSO4+SO2↑+2H2O反应中,
(1)请用双线桥法标出电子得失情况,______
(2)若有0.1mol Cu发生了反应,则转移的电子个数为______;若有0.1mol电子发生了转移,则所生成的SO2气体在标准状况下的体积为______.
题型:未知 难度:其他题型
答案
(1)该氧化还原反应中,得电子的元素是硫,化合价降低2价,失电子的元素是铜,化合价升高2价,所以转移电子2mol,如下所示:
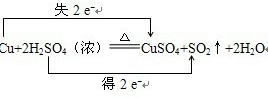
,故答案为:

;
(2)反应Cu+2H2SO4(浓) △ . CuSO4+SO2↑+2H2O中,消耗1mol铜,转移的电子是2mol,当有0.1molCu发生了反应,则转移电子0.2mol,个数为0.2mol×6.02×1023mol-1=1.202×1022,反应中转移的电子是2mol时,生成的SO2气体物质的量为1mol,当转移0.1mol电子时,则生成二氧化硫的物质的量是0.05mol,体积是:0.05mol×22.4L/mol=1.12L.
故答案为:1.202×1022;1.12L.
解析
△ .
考点
据考高分专家说,试题“在Cu+2H2SO4(浓)△.CuSO4.....”主要考查你对 [化学反应方程式 ]考点的理解。
化学反应方程式
化学方程式:
用化学式来表示化学反应的式子,叫做化学方程式。化学方程式不仅表明了反应物、生成物和反应条件,同时,通过相对分子质量或相对原子质量还可以表示个物质之间的质量关系,即各物质之间的质量比。
书写化学方程式要遵守两个原则:
一是必须以客观事实为基础,绝不能凭空臆想、臆造事实上不存在的物质和化学反应;
二是要遵守质量守恒定律,等号两边各原子种类与数目必须相等。
化学方程式的意义:
化学方程式不仅表明了反应物、生成物和反应条件。同时,化学计量数代表了各反应物、生成物物质的量关系,通过相对分子质量或相对原子质量还可以表示各物质之间的质量关系,即各物质之间的质量比。对于气体反应物、生成物,还可以直接通过化学计量数得出体积比。




