题文
用于金属焊接的某种焊条,其药皮由大理石、水泥、硅铁等配制而成.
(1)Al的原子结构示意图为______;Al与NaOH溶液反应的离子方程式为______.
(2)30Si原子的中子数为______,SiO2的晶体类型为______.
(3)Al3+与Yn-的电子数相同,Y所在族各元素的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是______.
(4)焊接过程中,药皮在高温下产生了熔渣和使金属不被氧化的气体,该气体是______.
(5)经处理后的熔渣36.0g(仅含Fe2O3、Al2O3、SiO2)加入足量稀盐酸,分离得到11.0g固体,滤液中加入过量NaOH溶液,分离得到21.4g固体.则此熔渣中Al2O3的质量分数为______.
题型:未知 难度:其他题型
答案
(1)铝原子的原子结构示意图为
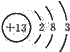
,铝和氢氧化钠、水反应生成偏铝酸钠和氢气,发生的离子反应方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑,故答案为:
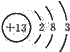
;2Al+2OH-+2H2O═2AlO2-+3H2↑;
(2)中子数=质量数-质子数=30-14=16,二氧化硅晶体中含有硅原子和氧原子,原子间以共价键形成空间网状结构,属于原子晶体,故答案为:16;原子晶体;
(3)Al3+与Yn-的电子数相同,Y所在族各元素的氢化物的水溶液均显酸性,则Y是第VIIA元素,氢化物的沸点随着相对分子质量的增大而增大,但HF中含有氢键导致HF的沸点大于HCl,所以该族氢化物中沸点最低的是HCl,
故答案为:HCl;
(4)高温下,大理石分解生成气体CO2,所以该气体是二氧化碳,故答案为:CO2;
(5)36.0g(仅含Fe2O3、Al2O3、SiO2)加入足量稀盐酸,二氧化硅不和盐酸反应,所以分离得到11.0g的固体是二氧化硅;
滤液中加入过量NaOH溶液,分离得到21.4g固体是氢氧化铁,根据2160×21.4214Fe(OH)3→Fe2O3,氧化铁的质量=160×21.4214g=16g,氧化铝的质量=(36.0-11.0-16)g=9g,氧化铝的质量分数=9g36g×100%=25%,
故答案为:25%.
解析
160×21.4214
考点
据考高分专家说,试题“用于金属焊接的某种焊条,其药皮由大理石、.....”主要考查你对 [化学反应方程式 ]考点的理解。
化学反应方程式
化学方程式:
用化学式来表示化学反应的式子,叫做化学方程式。化学方程式不仅表明了反应物、生成物和反应条件,同时,通过相对分子质量或相对原子质量还可以表示个物质之间的质量关系,即各物质之间的质量比。
书写化学方程式要遵守两个原则:
一是必须以客观事实为基础,绝不能凭空臆想、臆造事实上不存在的物质和化学反应;
二是要遵守质量守恒定律,等号两边各原子种类与数目必须相等。
化学方程式的意义:
化学方程式不仅表明了反应物、生成物和反应条件。同时,化学计量数代表了各反应物、生成物物质的量关系,通过相对分子质量或相对原子质量还可以表示各物质之间的质量关系,即各物质之间的质量比。对于气体反应物、生成物,还可以直接通过化学计量数得出体积比。




