题文
如图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空
族
周期ⅠAⅡAⅢAⅣAⅤAⅥAⅦA0二①②三③④⑤⑥⑦⑧四⑨⑩(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为______
(2)在这些元素中,地壳中含量最多的金属元素是______
(3)用电子式表示②与④形成化合物的过程______.
(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是______,碱性最强的是______,呈两性的氢氧化物是______
(5)写出⑤与氢氧化钠溶液反应的化学方程式:______.
写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式:______.
(6)某元素R的气态氢化物为HXR,且R在该氢化物中的质量分数为94%,8.5g的HXR气体在标准状态下的体积是5.6L.则HXR的相对分子量为______;HXR的化学式为______.
题型:未知 难度:其他题型
答案
(1)因⑧是Ar元素,为惰性元素,化学性质稳定,其原子结构示意图为
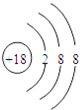
;
(2)地壳中元素含量从高到低的顺序为:氧、硅、铝、铁、钙、钠、钾、镁等;
(3)因②是F元素,④是Mg元素,所以MgF2的形成过程是:
(4)因非金属性元素最强的是Cl元素,金属性最强的元素是K元素,所以酸性最强的是HClO4,碱性最强的是KOH,两性的氢氧化物只有Al(OH)3;
(5)因⑤是铝,所以铝与氢氧化钠溶液反应以及氢氧化铝与氢氧化钠溶液反应的方程式分别为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,Al(OH)3+OH-=AlO2-+2H2O;
(6)HxR气体在标准状况下的体积是5.6L,说明物质的量为5.6/22.4=0.25mol,又因为气体质量为8.5g,所以摩尔质量为8.5/0.25=34因此HxR的相对分子质量为34,R在该氢化物中的质量分数为94%,所以R的原子量为34*0.94=31.96=32,所以R是硫,因此HxR的化学式为H2S.
故答案为:(1)

;
(2)Al;
(3)
(4)HClO4;KOH;Al(OH)3;
(5)2Al+2NaOH+2H2O=2NaAlO2+3H2↑,Al(OH)3+OH-=AlO2-+2H2O;
(6)34,H2S.
解析
该题暂无解析
考点
据考高分专家说,试题“如图是元素周期表的一部分,表中的①~⑩中.....”主要考查你对 [化学反应方程式 ]考点的理解。
化学反应方程式
化学方程式:
用化学式来表示化学反应的式子,叫做化学方程式。化学方程式不仅表明了反应物、生成物和反应条件,同时,通过相对分子质量或相对原子质量还可以表示个物质之间的质量关系,即各物质之间的质量比。
书写化学方程式要遵守两个原则:
一是必须以客观事实为基础,绝不能凭空臆想、臆造事实上不存在的物质和化学反应;
二是要遵守质量守恒定律,等号两边各原子种类与数目必须相等。
化学方程式的意义:
化学方程式不仅表明了反应物、生成物和反应条件。同时,化学计量数代表了各反应物、生成物物质的量关系,通过相对分子质量或相对原子质量还可以表示各物质之间的质量关系,即各物质之间的质量比。对于气体反应物、生成物,还可以直接通过化学计量数得出体积比。




