题文
取等物质的量浓度的NaOH溶液两份,每份50mL.向其中分别通入一定量的CO2气体,随后各取溶液10mL,并分别加水稀释到100mL.分别向稀溶液后的溶液中逐滴加入0.1mol/L的盐酸,产生CO2气体的体积(标准状况)与所加入的盐酸的体积之间的关系如图(a)(b)所示.回答下列问题: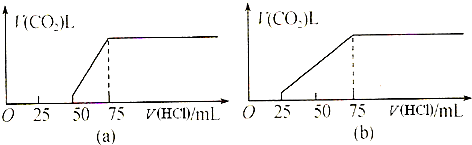
(1)在(a)情况下,溶质为(写化学式)______,其物质的量之比是______
(2)在(b)情况下,溶质为(写化学式)______,标准状况下,通入CO2气体的体积为______.
(3)原NaOH溶液中溶质的物质的量的浓度为______.
题型:未知 难度:其他题型
答案
当生成CO2气体时,发生反应NaHCO3+HCl=NaCl+H2O+CO2↑,
(1)(a)中生成CO2气体至最大,消耗HCl为25mL,若二氧化碳与NaOH反应后溶液中不含NaHCO3,由Na2CO3+HCl=NaHCO3+NaCl可知,将CO32-转化为HCO3-应消耗HCl为25mL,而图象中开始生成CO2气体时消耗HCl体积为50mL,说明该阶段还发生反应NaOH+HCl=NaCl+H2O,溶液中溶质为NaOH、Na2CO3,中和NaOH消耗HCl的体积为50mL-25mL=25mL,
由方程式可知NaHCO3和Na2CO3的物质的量之比等于两个过程分别消耗盐酸的体积之比,故NaOH、Na2CO3的物质的量之比=25mL:25mL=1:1,
故答案为:NaOH、Na2CO3;1:1;
(2)(b)中生成CO2气体至最大,消耗HCl为50mL,若二氧化碳与NaOH反应后溶液中不含NaHCO3,由Na2CO3+HCl=NaHCO3+NaCl可知,将CO32-转化为HCO3-应消耗HCl为50mL,而图象中开始生成CO2气体时消耗HCl体积为25mL,说明该阶段只发生Na2CO3+HCl=NaHCO3+NaCl,且二氧化碳与NaOH反应后溶液中含NaHCO3、Na2CO3,
根据碳元素守恒可知,从25mL~75mL消耗50mL盐酸时生成的二氧化碳为10mLNaOH溶液通入CO2气体的体积,该阶段生成二氧化碳为0.05L×0.1mol/L=0.005mol,故50mLNaOH溶液中通入二氧化碳的体积=0.005mol/L×50ml10ml×22.4L/mol=0.56L,
故答案为:NaHCO3、Na2CO3;0.56L;
(3)加入75mL盐酸时,溶液中溶质都恰好完全反应,此时溶液为NaCl溶液,根据守恒可知10mL溶液中n(NaOH)=n(NaCl)=n(HCl)=0.075L×0.1mol/L=0.0075mol,故原氢氧化钠溶液的浓度=0.0075mol0.01L=0.75mol/L,故答案为:0.75mol/L.
解析
50ml10ml
考点
据考高分专家说,试题“取等物质的量浓度的NaOH溶液两份,每份.....”主要考查你对 [化学反应方程式 ]考点的理解。
化学反应方程式
化学方程式:
用化学式来表示化学反应的式子,叫做化学方程式。化学方程式不仅表明了反应物、生成物和反应条件,同时,通过相对分子质量或相对原子质量还可以表示个物质之间的质量关系,即各物质之间的质量比。
书写化学方程式要遵守两个原则:
一是必须以客观事实为基础,绝不能凭空臆想、臆造事实上不存在的物质和化学反应;
二是要遵守质量守恒定律,等号两边各原子种类与数目必须相等。
化学方程式的意义:
化学方程式不仅表明了反应物、生成物和反应条件。同时,化学计量数代表了各反应物、生成物物质的量关系,通过相对分子质量或相对原子质量还可以表示各物质之间的质量关系,即各物质之间的质量比。对于气体反应物、生成物,还可以直接通过化学计量数得出体积比。




