题文
实验室里通常用MnO2与浓盐酸在加热的条件下反应制取氯气,为进行有关氯气的性质实验,需要4瓶容积为100ml的氯气(标准状况).
(1)写出实验室制取氯气的化学反应方程式并标出电子转移的方向及数目.
(2)制取4瓶氯气,理论上需要MnO2固体的质量是多少?(浓盐酸过量,并可以补充)
(3)实际称量的MnO2固体的质量必需多于理论量,主要原因是什么?
题型:未知 难度:其他题型
答案
(1)反应方程式为MnO2+4HCl(浓)△.MnCl2+Cl2↑+2H2O,转移电子数为2e-,用双线桥表示电子转移数目与方向为: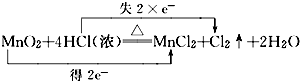
,
答:实验室制取氯气的化学反应方程式并标出电子转移的方向及数目为: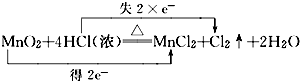
.
(2)氯气的物质的量=0.4L22.4L/mol=156mol,根据方程式MnO2+4HCl(浓)△.MnCl2+Cl2↑+2H2O可知,需要二氧化锰的物质的量=156mol,故需要二氧化锰的质量=156mol×87g/mol=1.55g,
答:需要二氧化锰的质量为1.55g.
(3)所产生的氯气不可能完全被收集、利用,故实际称量的MnO2固体的质量必需多于理论量,
答:实际称量的MnO2固体的质量必需多于理论量的主要原因是:所产生的氯气不可能完全被收集、利用.
解析
△.
考点
据考高分专家说,试题“实验室里通常用MnO2与浓盐酸在加热的条.....”主要考查你对 [化学反应方程式 ]考点的理解。
化学反应方程式
化学方程式:
用化学式来表示化学反应的式子,叫做化学方程式。化学方程式不仅表明了反应物、生成物和反应条件,同时,通过相对分子质量或相对原子质量还可以表示个物质之间的质量关系,即各物质之间的质量比。
书写化学方程式要遵守两个原则:
一是必须以客观事实为基础,绝不能凭空臆想、臆造事实上不存在的物质和化学反应;
二是要遵守质量守恒定律,等号两边各原子种类与数目必须相等。
化学方程式的意义:
化学方程式不仅表明了反应物、生成物和反应条件。同时,化学计量数代表了各反应物、生成物物质的量关系,通过相对分子质量或相对原子质量还可以表示各物质之间的质量关系,即各物质之间的质量比。对于气体反应物、生成物,还可以直接通过化学计量数得出体积比。




