题文
(11分)直接排放含二氧化硫、氮氧化物均会危害环境,必须对它们进行处理。
⑴利用钠碱循环法可脱除烟气中的SO2。
①用化学方程式表示SO2形成硫酸型酸雨的反应:
。
②在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反
应的离子方程式是_________ 。
⑵处理氮氧化物的方法很多,以下列举几种常见方法。
①用过量NaOH溶液吸收NO2气体。所得溶液中除含有NaOH和NaNO2,还含有
。
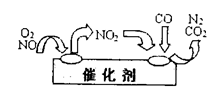
②为避免污染,常给汽车安装尾气净化装置。净化装置里装有催化剂,气体在催化剂表面吸附与解吸作用的机理如下图所示。写出净化过程中的总化学反应方程式:
。
③用氨气可以将其转化为无害气体,发生的 反应为:6NOx+4xNH3=(3+2x)N2+6xH2O。某工厂排出的尾气中NOx的含量为0.56%(体积分数), 若处理1×104L(标准状况)该尾气需42.5gNH3,则x= 。
题型:未知 难度:其他题型
答案
(1)①SO2+H2O=H2SO3 2H2SO3+O2=2H2SO4(2分)
②SO2+2OH¯=SO2-3+H2O(2分)
⑵①NaNO3(2分)②2NO+O2+4CO
4CO2+N2(2分)③1.5(3分)
解析
(1)①酸雨的形成主要是由于空气中的SO2溶于雨水形成的。发生的反应为:SO2+H2O=H2SO3 2H2SO3+O2=2H2SO4。②SO2与NaOH溶液反应的离子方程式为:SO2+2OH¯=SO2-3+H2O。
(2)①发生反应的化学方程式为:2NaOH+2NO2=NaNO2+NaNO3+H2O。因此另一种溶质为NaNO3。②发生反应的化学方程式为:2NO+O2+4CO
4CO2+N2。
③1×104L(标准状况)该尾气中
,42.5gNH3的物质的量
,由化学方程式可得比例式: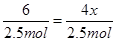
,解得
。
点评:本题属于基础题,考生必须掌握。在书写化学方程式时,应注意配平。
考点
据考高分专家说,试题“(11分)直接排放含二氧化硫、氮氧化物均.....”主要考查你对 [质量守恒定律 ]考点的理解。
质量守恒定律
质量守恒定律:
参加化学反应的各物质质量总和等于反应后生成的各物质质量总和。
化学反应前后,各种原子种类、数目、质量都不改变。
任何变化包括化学反应和核反应都不能消除物质,只是改变了物质的原有形态或结构,所以该定律又称物质不灭定律。
质量守恒定律的本质:
原子是物质质量的最小承担者。故在化学反应中,只要各种原子总数保持不变,则总质量保持不变。所以,质量守恒定律也就等价于元素守恒。
质量守恒定律的适用范围:
①质量守恒定律适用的范围是化学变化而不是物理变化;
②质量守恒定律揭示的是质量守恒而不是其他方面的守恒。物体体积不一定守恒;
③质量守恒定律中“参加反应的”不是各物质质量的简单相加,而是指真正参与了反应的那一部分质量,反应物中可能有一部分没有参与反应;
④质量守恒定律的推论:化学反应中,反应前各物质的总质量等于反应后各物质的总质量
质量守恒定律的应用:
(1)根据质量守恒定律,参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。利用这一定律可以解释反应前后物质的质量变化及用质量差确定某反应物或生成物的质量。
(2)根据质量守恒定律,化学反应前后元素的种类和质量不变,由此可以推断反应物或生成物的组成元素。
(3)据质量守恒定律:化学反应前后元素的种类和数目相等,推断反应物或生成物的化学式。
(4)已知某反应物或生成物质量,根据化学方程式中各物质的质量比,可求出生成物或反应物的质量。




