题文
阅读下列材料后回答问题。
一个体重60 kg健康的成年人,体内约含有4 g铁,这4 g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+转化为Fe2+,有利于人体吸收。
(1)在人体中进行Fe2+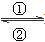
Fe3+的转化时, ①中的Fe2+作________剂,②中的Fe3+作___________剂。
(2)“服用维生素C,可使食物中的Fe3+转化为Fe2+”这句话指出,维生素C在这一反应中作___________剂,具有___________性。
(3)市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐。此反应的离子方程式为_______________
(并用单线桥法标出该式中的电子转移方向和数目)。
题型:未知 难度:其他题型
答案
(1)①还原剂 ②氧化剂
(2)还原剂 还原性
(3)Fe + 2H+ = Fe2+ + H2↑
单线桥转移2e-
解析
(1)Fe2+→Fe3+的转化时,元素的化合价升高,作还原剂;Fe3+→Fe2+转化时,元素的化合价降低,作氧化剂;(2)维生素C,可使食物中的Fe3+还原成Fe2+,Fe元素的化合价降低,作氧化剂,则维生素C具有还原性,作还原剂。(3)铁粉在人体胃酸(主要成分时盐酸)的作用下转化成亚铁盐的化学反应为Fe + 2H+ = Fe2+ + H2↑。
考点
据考高分专家说,试题“阅读下列材料后回答问题。一个体重60 k.....”主要考查你对 [质量守恒定律 ]考点的理解。
质量守恒定律
质量守恒定律:
参加化学反应的各物质质量总和等于反应后生成的各物质质量总和。
化学反应前后,各种原子种类、数目、质量都不改变。
任何变化包括化学反应和核反应都不能消除物质,只是改变了物质的原有形态或结构,所以该定律又称物质不灭定律。
质量守恒定律的本质:
原子是物质质量的最小承担者。故在化学反应中,只要各种原子总数保持不变,则总质量保持不变。所以,质量守恒定律也就等价于元素守恒。
质量守恒定律的适用范围:
①质量守恒定律适用的范围是化学变化而不是物理变化;
②质量守恒定律揭示的是质量守恒而不是其他方面的守恒。物体体积不一定守恒;
③质量守恒定律中“参加反应的”不是各物质质量的简单相加,而是指真正参与了反应的那一部分质量,反应物中可能有一部分没有参与反应;
④质量守恒定律的推论:化学反应中,反应前各物质的总质量等于反应后各物质的总质量
质量守恒定律的应用:
(1)根据质量守恒定律,参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。利用这一定律可以解释反应前后物质的质量变化及用质量差确定某反应物或生成物的质量。
(2)根据质量守恒定律,化学反应前后元素的种类和质量不变,由此可以推断反应物或生成物的组成元素。
(3)据质量守恒定律:化学反应前后元素的种类和数目相等,推断反应物或生成物的化学式。
(4)已知某反应物或生成物质量,根据化学方程式中各物质的质量比,可求出生成物或反应物的质量。




