题文
已知氧化还原反应与四种基本反应类型的关系可用如图表示,下列是有水参加或生成的几种反应: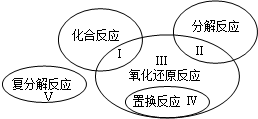
①CaO+H2O =Ca(OH)2
②2Na+H2O=2NaOH+H2↑
③H2+CuO 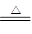
Cu +H2O
④3S+6NaOH 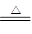
2Na2S +Na2SO3 +3H2O
⑤NaOH+HCl=NaCl+H2O
请回答下列问题:
(1)反应①中水 (填字母)。A.是氧化剂B.是还原剂C.既是氧化剂又是还原剂D.既不是氧化剂又不是还原剂(2)反应③被氧化的元素是 (填元素符号)。
(3)上述反应中,属于区域Ⅲ的是 (填序号)。
(4)写出一种符合区域Ⅴ且既有沉淀生成又有水生成的离子方程式: 。
题型:未知 难度:其他题型
答案
(1)D (2)H (3)④
(4)H2CO3+Ca2++2OH-=CaCO3+2H2O(只要符合题意:既有沉淀生成又有水生成的复分解反应的离子方程式)
解析
(1)CaO+H2O =Ca(OH)2该反应中,水所含的H、O元素化合价均为改变,故水既不是氧化剂又不是还原剂。选择D选项。(2)H2+CuO 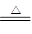
Cu +H2O根据反应可知,H元素化合价升高,Cu元素化合价降低,故被氧化的元素为H元素。(3)Ⅲ区域为氧化还原反应,且不属于置换、化合、分解反应,故④符合题意。(4)Ⅴ区域为复分解反应,且有沉淀,水生成。H2CO3+Ca2++2OH-=CaCO3+2H2O
考点
据考高分专家说,试题“已知氧化还原反应与四种基本反应类型的关系.....”主要考查你对 [质量守恒定律 ]考点的理解。
质量守恒定律
质量守恒定律:
参加化学反应的各物质质量总和等于反应后生成的各物质质量总和。
化学反应前后,各种原子种类、数目、质量都不改变。
任何变化包括化学反应和核反应都不能消除物质,只是改变了物质的原有形态或结构,所以该定律又称物质不灭定律。
质量守恒定律的本质:
原子是物质质量的最小承担者。故在化学反应中,只要各种原子总数保持不变,则总质量保持不变。所以,质量守恒定律也就等价于元素守恒。
质量守恒定律的适用范围:
①质量守恒定律适用的范围是化学变化而不是物理变化;
②质量守恒定律揭示的是质量守恒而不是其他方面的守恒。物体体积不一定守恒;
③质量守恒定律中“参加反应的”不是各物质质量的简单相加,而是指真正参与了反应的那一部分质量,反应物中可能有一部分没有参与反应;
④质量守恒定律的推论:化学反应中,反应前各物质的总质量等于反应后各物质的总质量
质量守恒定律的应用:
(1)根据质量守恒定律,参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。利用这一定律可以解释反应前后物质的质量变化及用质量差确定某反应物或生成物的质量。
(2)根据质量守恒定律,化学反应前后元素的种类和质量不变,由此可以推断反应物或生成物的组成元素。
(3)据质量守恒定律:化学反应前后元素的种类和数目相等,推断反应物或生成物的化学式。
(4)已知某反应物或生成物质量,根据化学方程式中各物质的质量比,可求出生成物或反应物的质量。




