题文
化学在环境保护中起着十分重要的作用。催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染。
(1)催化反硝化法中,H2能将NO3-还原为N2。25℃时,反应进行l0 min,溶液的pH由7变为l 2。
①N2的结构式为
②上述反应的离子方程式为 ,其平均反应速率v(NO3-)为 mol·L-1·min-1。
③还原过程中可生成中间产物NO2-,写出2种促进NO2-水解的方法 。
(2)电化学降解NO3-的原理如下图所示。
①电源正极为 (填“A”或“B”),阴极反应式为:
②若电解过程中转移了2 mol电子,则膜两侧电解液的质量变化差(△m左-△m右)为 g。
题型:未知 难度:其他题型
答案
(1)①N≡N 2NO3-+5H2
N2+2OH-+4H2O 0.001mol/(L·min)
③加酸,升高温度,加水
(2)A, 2NO3-+6H2O+10e-=N2+12OH- ②14.4
解析
(1) ②废水不应显酸性(HNO3易挥发),而是中性或碱性,所以O2-在水中以H2O或OH-形式存在,有题意也可看出生成OH-(溶液pH由7变为12),依据氧化还原反应规律可配平: 
pH=12
c(H+)=1×10-12mol·L-1
c(OH-)= 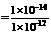
1×10-2mol·L-1
υ(NO3-)=υ(OH-)= 1×10-10mol·L-1 /10min= 0.001mol·L-1·min-1
③由方程式知NO2-+H2O
HNO2+OH-△H>0 ,加热,加酸均可均可使平衡正向移动,促进NO2-转化。
(2)①2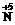
O3-+10e-→
+6O2,所以B极为电源负极,A极为电源正极。
O2-+H2O=2OH-,可以写出阴极反应式:2NO3-+6H2O+10e-= N2↑+12OH-
② 左(+)阳极:4H2O(OH-)-4e-=4H++O2↑+2H2O
右(- )阴极:2NO3-+6H2O+10e-= N2↑+12OH-
10 e-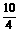
O2(左)- 1N2(右)-10H+
10mol 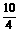
mol 1mol 10mol
2mol 0.5mol 0.2mol 2mol
由于阴阳极之间被质子交换膜隔开,左侧电解产生的H+会穿过质子交换膜进入右侧,所以:
△m左=m(O2)+m(H+)=0.5mol×32g·mol-1+2mol×1g·mol-1="18g"
△m右= m(N2)-m(H+)=0.2mol×28g·mol-1-2mol×1g·mol-1=3.6g
△m左-△m右="18g-3.6g" = 14.4g
考点
据考高分专家说,试题“化学在环境保护中起着十分重要的作用。催化.....”主要考查你对 [质量守恒定律 ]考点的理解。
质量守恒定律
质量守恒定律:
参加化学反应的各物质质量总和等于反应后生成的各物质质量总和。
化学反应前后,各种原子种类、数目、质量都不改变。
任何变化包括化学反应和核反应都不能消除物质,只是改变了物质的原有形态或结构,所以该定律又称物质不灭定律。
质量守恒定律的本质:
原子是物质质量的最小承担者。故在化学反应中,只要各种原子总数保持不变,则总质量保持不变。所以,质量守恒定律也就等价于元素守恒。
质量守恒定律的适用范围:
①质量守恒定律适用的范围是化学变化而不是物理变化;
②质量守恒定律揭示的是质量守恒而不是其他方面的守恒。物体体积不一定守恒;
③质量守恒定律中“参加反应的”不是各物质质量的简单相加,而是指真正参与了反应的那一部分质量,反应物中可能有一部分没有参与反应;
④质量守恒定律的推论:化学反应中,反应前各物质的总质量等于反应后各物质的总质量
质量守恒定律的应用:
(1)根据质量守恒定律,参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。利用这一定律可以解释反应前后物质的质量变化及用质量差确定某反应物或生成物的质量。
(2)根据质量守恒定律,化学反应前后元素的种类和质量不变,由此可以推断反应物或生成物的组成元素。
(3)据质量守恒定律:化学反应前后元素的种类和数目相等,推断反应物或生成物的化学式。
(4)已知某反应物或生成物质量,根据化学方程式中各物质的质量比,可求出生成物或反应物的质量。




