题文
Ⅰ.某溶液中仅含下表离子中的5种离子(不考虑水的电离及离子的水解),且离子的物质的量均为1mol。
阴离子
SO42-、NO3-、Cl-
阳离子
Fe3+、Fe2+、NH4+、Cu2+、Al3+
①若向原溶液中加入KSCN溶液,无明显变化。②若向原溶液中加入过量的盐酸,有气体生成,溶液中阴离子种类不变。③若向原溶液中加入BaCl2溶液,有白色沉淀生成。试回答下列问题
(1)若先向原溶液中加入过量的盐酸,再加入KSCN溶液,现象是 。
(2)原溶液中含有的阳离子是 。
(3)向原溶液中加入足量的盐酸,发生反应的离子方程式为 。
(4)向原溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体用托盘天平称量质量为 。
Ⅱ. 草酸亚铁晶体(FeC2O4·2H2O)、碳酸锂和二氧化硅在氩气中高温反应可制备锂电池的正极材料硅酸亚铁锂(Li2FeSiO4)。草酸亚铁晶体在氩气气氛中进行热重分析,结果如右图所示(TG%表示残留固体质量占原样品总质量的百分数),请回答下列问题:
(5)草酸亚铁晶体中碳元素的化合价为:
(6)A→B发生反应的化学方程式为 。
(7)精确研究表明,B→C实际是分两步进行的,每一步只释放一种气体,第二步释放的气体的相对分子质量较第一步的大,则第一步释放的气体化学式为: ;释放第二种气体时,反应的化学方程式为 。
题型:未知 难度:其他题型
答案
(16分,每空2分)(1)溶液呈红色(2分) (2)Fe2+、Cu2+ (2分);
(3)3Fe2++4H++NO3-=3Fe3++NO↑+2H2O(2分) (4)160.0g(2分)(写成160g不给分);
(5)+3(2分) (6)FeC2O4·2H2O
FeC2O4 +2H2O(2分)
(7)CO(2分) FeCO3
FeO + CO2↑(2分)
解析
Ⅰ.若向溶液中加入KSCN溶液,无明显变化,说明原溶液中不含Fe3+;若向溶液中加入过量的盐酸,有气体生成,溶液中阴离子种类不变,说明原溶液中含有Cl-,该气体只能是NO,说明含有具有氧化性的NO3-和具有还原性的Fe2+。若向溶液中加入BaCl2溶液,有白色沉淀生成,说明原溶液中含有SO42-。各离子的物质的量均为1mol,因此根据电荷守恒可知还应含有Cu2+,所以原溶液中所含阳离子是Fe2+、Cu2+,阴离子是NO3-、Cl-、SO42-。
(1)如果先加入盐酸,在酸性条件下NO3-具有氧化性,能和具有还原性的Fe2+发生氧化还原反应,反应的离子方程式为3Fe2++4H++NO3-=3Fe3++NO↑+2H2O。所以再滴入KSCN溶液,溶液呈红色。
(2)原溶液中含有的阳离子是Fe2+和Cu2+。
(3)根据以上分析可知,向原溶液中加入足量的盐酸,发生反应的离子方程式为3Fe2++4H++NO3-=3Fe3++NO↑+2H2O。
(4)原溶液中所含阳离子是Fe2+、Cu2+,若向原溶液中加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,最终得到的固体应该是是CuO、Fe2O3。根据题意各离子的物质的量均为1mol可知,m(CuO)=1.0mol×80g/mol=80.0g,m(Fe2O3)=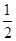
×1.0mol×160g/mol=80.0g,所得固体的质量为80.0g+80.0g=160.0g。
Ⅱ.(5)草酸亚铁晶体(FeC2O4·2H2O)中铁元素的化合价是+2价,氧元素是-2价,所以碳元素的化合价是(2×4-2)÷2=+3价。
(6)根据草酸亚铁晶体的化学式FeC2O4·2H2O可知,晶体中结晶水的含量是
×100%=20%,所以A→B发生反应恰好是失去结晶水,因此反应的化学方程式为FeC2O4·2H2O
FeC2O4 +2H2O。
(7)草酸亚铁晶体中FeO的含量是
×100%=40%,所以C点生成的固体是氧化亚铁。由于第二步释放的气体的相对分子质量较第一步的大,所以第一步释放的是CO,第二步释放的是CO2,反应的化学方程式分别是FeC2O4
FeCO3+CO、FeCO3
FeO + CO2↑。
考点
据考高分专家说,试题“Ⅰ.某溶液中仅含下表离子中的5种离子(不.....”主要考查你对 [离子共存 ]考点的理解。
离子共存
离子共存:
所谓离子共存实质上就是看离子间是否发生反应。若离子在溶液中发生反应,就不能共存。
因能发生氧化还原反应而不共存的离子有:
(注:“√”表示能发生反应,“×”表示不能发生反应)
S2-
SO32-
I-
Fe2+
Br-
Cl-(H+)
MnO4-
√
√
√
√
√
√
ClO-
√
√
√
√
√
√
NO3-(H+)
√
√
√
√
√
×
Fe3+
√
√
√
×
×
×
因能发生复分解反应而不共存的离子有:
- 离子间相互结合生成难溶物或微溶物
Ba2+、Ca2+CO32-、SO32-、SO42-Ag+CO32-、SO32-、Cl- - 离子间相互结合生成气体或挥发性物质
H+CO32-、HCO3-、SO32-、HSO3-、S2-、HS-OH-NH4+ - 离子间相互结合生成弱电解质
H+ CO32-、SO32-、S2-、CH3COO-、F-弱酸OH-NH4+、Al3+、Fe3+、Cu2+、Mg2+弱碱H+水
因能发生双水解的离子有:
Al3+CO32-、HCO3-、SO32-、HSO3-、S2-、HS-、AlO2-、ClO-Fe3+CO32-、HCO3-、AlO2-、ClO-NH4+SiO32-、AlO2-
因发生络合反应而不共存的离子有:
Fe3+ SCN-Ag+、Cu2+NH3·H2O
null
null
null
判断离子是否共存的几种情况:
(1)发生复分解反应,离子不能大量共存。
①有气体产生 如CO32-、SO32-、S2-、HCO3-、HSO3-、HS-等易挥发的弱酸的酸根与H+不能大量共存。
②有沉淀生成 如Ba2+、Ca2+、Mg2+、Ag+等不能与SO42-、CO32-等大量共存;
Mg2+、Fe2+、Ag+、Al3+、Zn2+、Cu2+、Fe3+等不能与OH-大量共存;
Pb2+与Cl-,Fe2+与S2-、Ca2+与PO43-、Ag+与I-不能大量共存。
③有弱电解质生成 如OH-、CH3COO-、PO43-、HPO42-、H2PO4-、F-、ClO-、AlO2-、SiO32-、CN-、C17H35COO-与H+不能大量共存;
一些酸式弱酸根如HCO3-、HPO42-、HS-、H2PO4-、HSO3-不能与OH-大量共存;
NH4+与OH-不能大量共存。
(2)发生氧化还原反应,离子不能大量共存
①具有较强还原性的离子不能与具有较强氧化性的离子大量共存 如S2-、HS-、SO32-、I-和Fe3+不能大量共存。
②在酸性或碱性的介质中由于发生氧化还原反应而不能大量共存 如MnO4-、Cr2O7-、NO3-、ClO-与S2-、HS-、SO32-、HSO3-、I-、Fe2+等不能大量共存;
SO32-和S2-在碱性条件下可以共存,但在酸性条件下由于发生2S2-+SO32-+6H+=3S↓+3H2O不能共存 ;H+与S2O32-不能大量共存。
(3)能水解的阳离子跟能水解的阴离子在水溶液中不能大量共存(双水解)
例:Al3+和HCO3-、CO32-、HS-、S2-、AlO2-、ClO-等;Fe3+与CO32-、HCO3-、AlO2-、ClO-等不能大量共存。
(4)溶液中能发生络合反应的离子不能大量共存。
如Fe2+、Fe3+与SCN-不能大量共存。
主要题目要求的限定:
(1)酸性溶液(H+)、碱性溶液(OH-)、能在加入铝粉后放出可燃气体的溶液、由水电离出的H+或OH-=1×10-10mol/L的溶液等。
(2)溶液的颜色:有色离子MnO4-(紫色)、Fe3+(棕黄)、Fe2+(浅绿)、Cu2+(蓝)、Fe(SCN)2+(红)、Fe(SCN)63-(血红)。
(3)要求“大量共存”还是“不能大量共存”。




