题文
下列图示与对应的叙述相符的是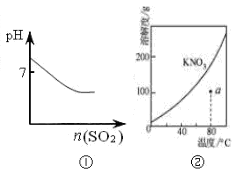
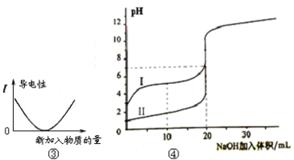
A.图①可表示将SO2气体通入溴水时pH的变化B.图②表示KNO3的溶解度曲线,a点是80 ℃的KNO3的不饱和溶液C.图③表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化D.图④表示室温下,0.100 mol/L NaOH 溶液分别滴定0.100 mol/L的盐酸和醋酸的滴定曲线,由图知Ⅰ为盐酸的滴定曲线。
题型:未知 难度:其他题型
答案
B
解析
A. SO2气体溶于水发生反应:SO2+H2O=H2SO3。H2SO3在水中电离产生大量的H+使溶液显酸性,PH<7,当通入溴水时,又发生反应:Br2+2H2O+SO2= SO42-+4H++2Br-.溶液的酸性进一步加强。错误。B. KNO3的溶解度随温度的升高而增大,在溶解度曲线上的点都是饱和溶液,在溶解度曲线左上方的点都是过饱和溶液,而在溶解度曲线右下方的点都是温度高,溶质还没有加到达到饱和所需要的质量,因此都是不饱和溶液。a点在溶解度曲线右下方,所以属于不饱和溶液。正确。C. 乙酸是弱电解质,在水中存在电离平衡:CH3COOH
CH3COO-+H+。所以乙酸溶液能导电。当向该溶液中通入氨气时发生反应:CH3COOH+NH3= CH3COONH4. CH3COONH4是强电解质在水中完全电离,自由移动的离子浓度大大增强,所以溶液的 导电性增强,当二者恰好完全反应时导电性基本达到最大值。因为氨气过量时与水反应得到的一水合氨是弱电解质,导电能力对该溶液来说没有很大的影响。因此错误。D.对于相同物质的量浓度的盐酸与醋酸来说,由于盐酸是强电解质,完全电离,醋酸是弱电解质,部分电离,所以H+的浓度盐酸的大。H+的浓度越大,溶液的PH越小。滴定过程中H+的浓度变化就越大。所以Ⅰ为醋酸的滴定曲线,Ⅱ为盐酸的滴定曲线。错误。
考点
据考高分专家说,试题“下列图示与对应的叙述相符的是A.图①可表.....”主要考查你对 [离子共存 ]考点的理解。
离子共存
离子共存:
所谓离子共存实质上就是看离子间是否发生反应。若离子在溶液中发生反应,就不能共存。
因能发生氧化还原反应而不共存的离子有:
(注:“√”表示能发生反应,“×”表示不能发生反应)
S2-
SO32-
I-
Fe2+
Br-
Cl-(H+)
MnO4-
√
√
√
√
√
√
ClO-
√
√
√
√
√
√
NO3-(H+)
√
√
√
√
√
×
Fe3+
√
√
√
×
×
×
因能发生复分解反应而不共存的离子有:
- 离子间相互结合生成难溶物或微溶物
Ba2+、Ca2+CO32-、SO32-、SO42-Ag+CO32-、SO32-、Cl- - 离子间相互结合生成气体或挥发性物质
H+CO32-、HCO3-、SO32-、HSO3-、S2-、HS-OH-NH4+ - 离子间相互结合生成弱电解质
H+ CO32-、SO32-、S2-、CH3COO-、F-弱酸OH-NH4+、Al3+、Fe3+、Cu2+、Mg2+弱碱H+水
因能发生双水解的离子有:
Al3+CO32-、HCO3-、SO32-、HSO3-、S2-、HS-、AlO2-、ClO-Fe3+CO32-、HCO3-、AlO2-、ClO-NH4+SiO32-、AlO2-
因发生络合反应而不共存的离子有:
Fe3+ SCN-Ag+、Cu2+NH3·H2O
null
null
null
判断离子是否共存的几种情况:
(1)发生复分解反应,离子不能大量共存。
①有气体产生 如CO32-、SO32-、S2-、HCO3-、HSO3-、HS-等易挥发的弱酸的酸根与H+不能大量共存。
②有沉淀生成 如Ba2+、Ca2+、Mg2+、Ag+等不能与SO42-、CO32-等大量共存;
Mg2+、Fe2+、Ag+、Al3+、Zn2+、Cu2+、Fe3+等不能与OH-大量共存;
Pb2+与Cl-,Fe2+与S2-、Ca2+与PO43-、Ag+与I-不能大量共存。
③有弱电解质生成 如OH-、CH3COO-、PO43-、HPO42-、H2PO4-、F-、ClO-、AlO2-、SiO32-、CN-、C17H35COO-与H+不能大量共存;
一些酸式弱酸根如HCO3-、HPO42-、HS-、H2PO4-、HSO3-不能与OH-大量共存;
NH4+与OH-不能大量共存。
(2)发生氧化还原反应,离子不能大量共存
①具有较强还原性的离子不能与具有较强氧化性的离子大量共存 如S2-、HS-、SO32-、I-和Fe3+不能大量共存。
②在酸性或碱性的介质中由于发生氧化还原反应而不能大量共存 如MnO4-、Cr2O7-、NO3-、ClO-与S2-、HS-、SO32-、HSO3-、I-、Fe2+等不能大量共存;
SO32-和S2-在碱性条件下可以共存,但在酸性条件下由于发生2S2-+SO32-+6H+=3S↓+3H2O不能共存 ;H+与S2O32-不能大量共存。
(3)能水解的阳离子跟能水解的阴离子在水溶液中不能大量共存(双水解)
例:Al3+和HCO3-、CO32-、HS-、S2-、AlO2-、ClO-等;Fe3+与CO32-、HCO3-、AlO2-、ClO-等不能大量共存。
(4)溶液中能发生络合反应的离子不能大量共存。
如Fe2+、Fe3+与SCN-不能大量共存。
主要题目要求的限定:
(1)酸性溶液(H+)、碱性溶液(OH-)、能在加入铝粉后放出可燃气体的溶液、由水电离出的H+或OH-=1×10-10mol/L的溶液等。
(2)溶液的颜色:有色离子MnO4-(紫色)、Fe3+(棕黄)、Fe2+(浅绿)、Cu2+(蓝)、Fe(SCN)2+(红)、Fe(SCN)63-(血红)。
(3)要求“大量共存”还是“不能大量共存”。




