1.硫的原子结构
硫元素位于元素周期表中第三周期第ⅥA族,最外层有6个电子,在化学反应中易获得2个电子而呈现出-2价。
自然界中硫元素的存在形式:
(2)硫的化学性质
单质硫的化合价为0,处于中间价态,故单质硫既有氧化性又有还原性,在反应中既可作氧化剂又可作还原剂。
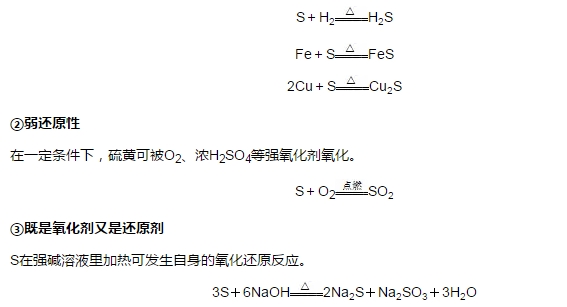
①弱氧化性
在加热的条件下,硫黄能被H2和绝大多数的金属单质还原。
【特别提醒】
①实验室中,残留在试管内壁上的硫可用CS2溶解除去,也可用热的NaOH溶液除去。
②硫单质的氧化性较弱,与变价金属反应时一般生成低价态金属硫化物(和Cl2与变价金属的反应情况相反),如FeS、Cu2S等。
③汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理。
④单质硫燃烧时,产物只能是SO2,无论O2的量是否充足,均不会生成SO3。
3.硫的应用
(1)制农药:如石硫合剂(石灰、硫黄)用于杀死果树的害虫。
文章来源于网络,由考高分网编辑整理,如有侵权请及时联系删除。