【核心知识梳理】
第1部分 原电池
一、原电池的工作原理
1.原电池定义
将化学能转化为电能的装置。
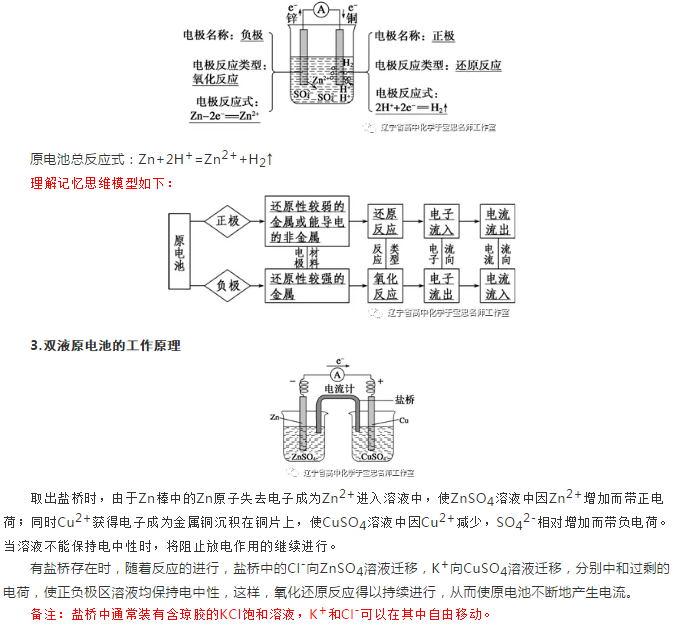
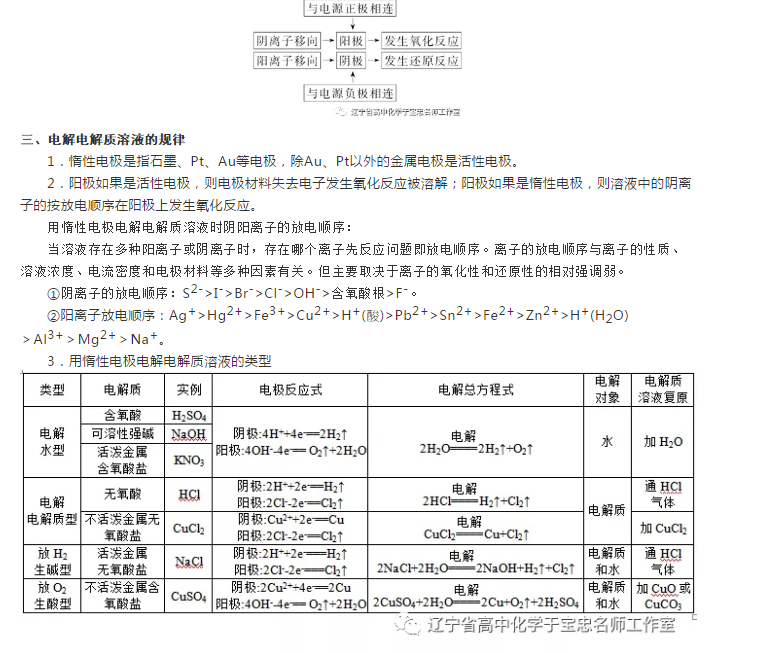
2.单液原电池的工作原理
原电池在工作时,负极失去电子,发生氧化反应,电子通过导线流向正极,溶液中氧化性物质得到电子,发生还原反应,从而在导线中不断有电子定向运动;在电解质溶液中,阳离子向正极运动,阴离子向负极运动;随着氧化还原反应的不断进行,从而在闭合回路中形成了电流,实现了化学能向电能的转化。
装置示意图如下:
4.原电池构成要素
(1)电极反应(可自发进行的氧化还原反应);
(2)电极材料(导体。单液电池二者活动性需不同);
(3)离子导体(电解质溶液、熔融电解质或离子交换膜);
(4)电子导体,并形成闭合回路。
二、原电池原理的应用
1.比较金属活动性
作负极的金属活动性强,作正极的金属活动性弱;
2.改变化学反应速率
如:在Zn和稀硫酸反应时,滴加少量CuSO4溶液,则Zn置换出的铜和锌能构成原电池的正负极,从而加快Zn与稀硫酸反应的速率;
3.设计原电池
(1)把氧化还原反应拆成氧化反应和还原反应两个半反应,从而确定电极反应。
(2)根据原电池的电极反应特点,结合两个半反应找出正负极材料及电解质溶液。
①负极材料:如发生氧化反应的物质为金属单质,可用该金属作电极材料;如为气体(如H-2)或溶液中的还原性离子,可用惰性电极(如Pt、石墨棒)作电极材料。
②正极材料:一般说来,应该选择比负极不活泼的金属,或非金属导体,或金属氧化物等作正极材料。
③电解质溶液:如果是单液原电池,一般选用总反应式中氧化剂溶液;如果是双液原电池,负极区选择氧化产物的溶液,正极区选择含氧化剂的溶液。
(3)画出装置的示意图,并根据要求用文字作必要的标注
【特别强调】
原电池正负极的判断方法
(1)根据组成原电池的两极材料判断
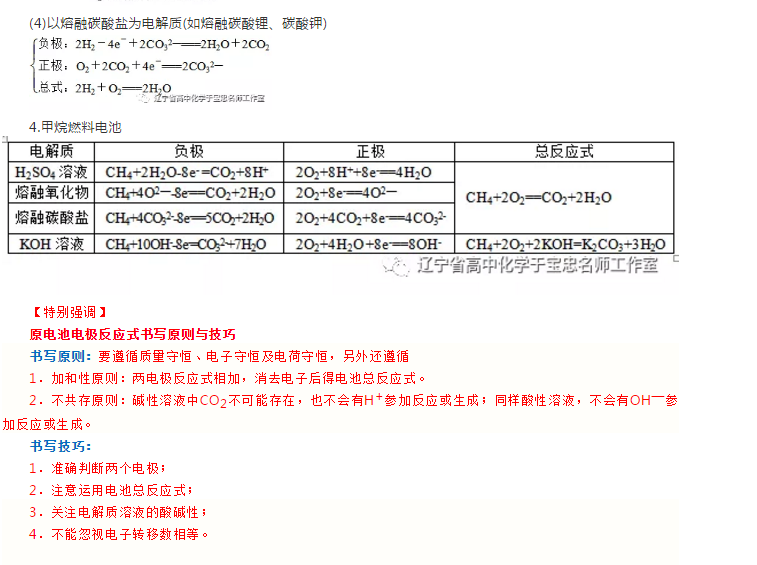
一般是活动性较强的金属为负极;活动性较弱的金属或能导电的非金属为正极。
(2)根据原电池两极发生的变化来判断
原电池的负极总是失电子发生氧化反应,正极总是得电子发生还原反应。
(3)根据电流方向或电子流动方向判断
电流是由正极流向负极;电子流动方向是由负极流向正极。
第3部分 电解池
一、电解
1.概念:使电流通过电解质溶液而在阴、阳两极引起氧化还原反应的过程。
2.特点
(1)电解是最强有力的氧化还原手段,是不可逆(填“可逆”或“不可逆”)的。
(2)电解质溶液的导电过程,就是电解质溶液的电解过程。
二、电解池
1.定义:把电能转化成化学能的装置。
2.电解池构成要素
(1)直流电源;
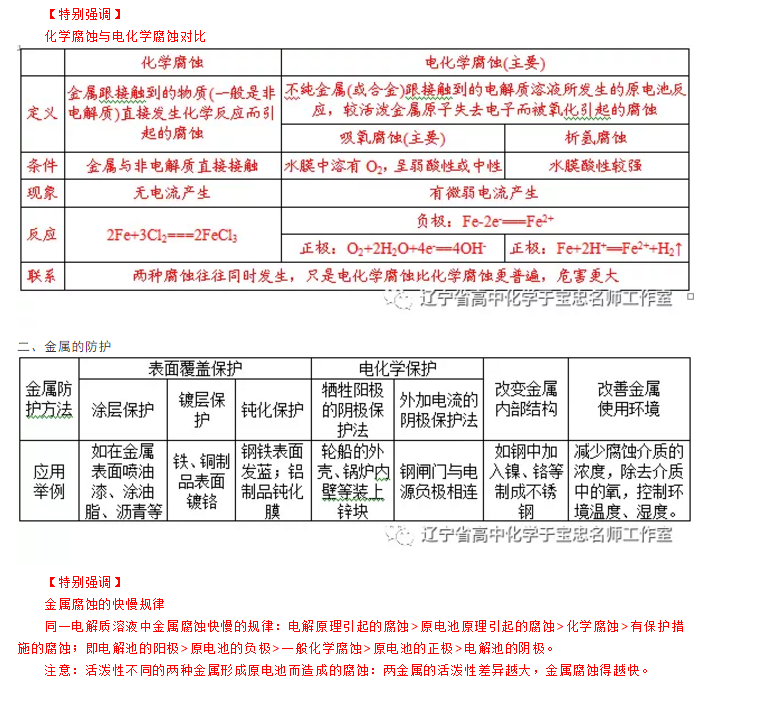
(2)两个电极:与电源正极相连的一极是阳极;与电源负极相连的一极是阴极;
(3)电解质溶液或熔融电解质;
(4)形成闭合回路。
3.电子流向和离子流向
(1)电子流向:电源负极―→电解池阴极
电解池阳极―→电源正极
(2)离子流向:阳离子―→电解池阴极
阴离子―→电解池阳极
【特别强调】
电解池阴、阳极的判断方法
在电解池中,阳离子向阴极移动,阴离子向阳极移动。判断方法归纳如下: