题文
铬的化合物有毒,由于+6价Cr的强氧化性,其毒性是+3价Cr毒性的100倍。因此,必须对含铬的废水进行处理。目前研究和采用的处理方法主要有:
方法一、还原法:
(Ⅰ)在酸性介质中用FeSO4、NaHSO3等将+6价Cr还原成+3价Cr。具体流程如下: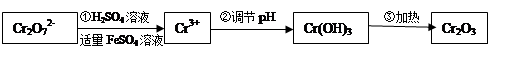
请回答下列问题:
(1)上述流程①发生反应的离子方程式是 。
(2)若在① 使FeSO4适当过量、空气适量,可产生具有磁性、组成类似于铁氧体(Fe3O4或FeO·Fe2O3)的复合氧化物(
·y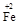
O)(注:X可以是分数),变废为宝。则控制空气适量的目的是 ,使铁氧体分离出来较简便的方法是 。假设处理含1 mol Cr2O72-的废水至少需要加入10mol FeSO4·7H2O则复合氧化物(
·y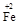
O)化学式是 。
(Ⅱ)研究发现,用铁粉作还原剂不仅可以除去Cr6+,还能除去废水中的少量Mn2+,现研究铁屑用量和pH值对废水中铬、锰去除率的影响,
(3)取100mL废水于250 mL三角瓶中,调节pH值到规定值,分别加入不同量的废铁屑.得到铁屑用量对铬和锰去除率的影响如下图1所示。则在pH一定时,废水中铁屑用量为 时锰、铬去除率最好
(4)取100mL废水于250 mL三角瓶中,加入规定量的铁粉,调成不同的pH值。得到pH值对铬和锰去除率的影响如下图2所示。则在铁屑用量一定时,废水pH= 时锰、铬去除率最好

方法二、电解法:将含+6价Cr的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解:阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3十在阴极区与OH一结合生成Fe(OH)3和Cr(OH)3沉淀除去。
(5)写出此阴极反应的电极方程式 。
(6)现用上法处理1×104 L含铬(+6价)78 mg / L的废水,电解时阳极物质消耗的质量至少为________kg。
题型:未知 难度:其他题型
答案
(16分)(1)Cr2O72-+14H++6Fe2+=6Fe3++2Cr3十+7H2O(2分))
(2)使溶液中的比例恰当(答防止Fe2+被氧气过度氧化可以给分)(2分)
用磁铁吸引(2分) Cr0.5Fe1.5O3·FeO(2分)
(3)15% (2分)(4) 4 (2分)(5)2H2O+2e-=H2↑+2OH-。 (2分) (6) 2.52 (2分)
解析
(1)Cr2O72-有较强氧化性,FeSO4中Fe2+有一定的还原性,在酸性介质中发生氧化还原反应,由实验流程可知,第①步反应中Cr2O72-在酸性条件下将Fe2+氧化为Fe3+,自身被还原为Cr3+,根据守恒元素守恒及所处环境可知,还应有水生成,反应离子方程式为Cr2O72-+14H++6Fe2+=2Cr3++6Fe3++7H2O。
(2)空气中含有氧气,如果空气过量,则Fe2+被氧气过度氧化,使溶液中Fe2+和Fe3+的比例不恰当。由于铁氧体具有磁性,所以使铁氧体分离出来较简便的方法是用磁铁吸引。根据反应的离子方程式可知,1mol Cr2O72-能氧化6mol亚铁离子,同时生成2mol Cr3十,而剩余亚铁离子的物质的量是4mol,所以根据原子守恒和化合价代数和为0可知,
、3x+6-3x+2y=8,解得x=0.5、y=1,所以复合氧化物的化学式是Cr0.5Fe1.5O3·FeO。
(3)根据图1知,当铁用量逐渐增大时,离子的去除率先增大后减小,当废水中铁屑用量为15%时锰、铬去除率最好。
(4)根据图2知,当溶液的pH值逐渐增大时,锰离子的去除率先减小后增大,铬的去除率先增大后减小,当pH=4时锰、铬去除率最好。
(5)电解池中阴极得到电子,则阴极是水电离出的氢离子得到电子,所以阴极反应的电极方程式2H2O+2e-=H2↑+2OH-。
(6)1×104 L含铬(+6价)78 mg / L的废水中铬元素的质量是78 mg / L×10000=780000mg=780g,物质的量是780g÷52g/mol=15mol。在反应中得到15mo×3=45mol电子,因此根据电子的得失守恒可知,参加反应的亚铁离子是45mol,所以阳极消耗铁的质量至少是45mol×56g/mol=2520g=2.52kg。
点评:本题以工业废水处理为载体,考查氧化还原反应、离子反应、电极反应式的书写以及有关计算等,难度中等,关键根据实验流程利用氧化还原反应判断发生的离子反应,是对学生综合能力的考查.是一道不错的能力考查题,有利于培养学生的逻辑推理能力和发散思维能力,也有助于培养学生的环境保护意识,提升学生的学科素养。
考点
据考高分专家说,试题“铬的化合物有毒,由于+6价Cr的强氧化性.....”主要考查你对 [离子反应 ]考点的理解。
离子反应
定义:
凡是有离子参加或离子生成的反应都是离子反应。
离子反应包括:复分解反应、氧化还原反应、络合反应、双水解反应
常见阳离子的检验方法:
离子检验试剂实验步骤实验现象离子方程式 K+焰色反应①铂丝在火焰上灼烧至原火焰色②蘸取溶液,放在火焰上灼烧,观察火焰颜色。浅紫色(通过蓝色钴玻璃片观察钾离子焰色)——Na+焰色反应火焰分别呈黄色NH4+NaOH溶液(浓)向未知溶液中加入NaOH浓溶液并加热生成有刺激性气味、使湿润红色石蕊试纸变蓝的气体NH4++OH-=NH3↑+H2OAl3+加NaOH溶液向未知溶液中加入NaOH溶液加入适量NaOH溶液后生成白色沉淀,该沉淀溶于过量NaOH溶液中
Al3++3OH-=Al(OH)3↓
Cu2+浓氨水向未知溶液中加入浓氨水加入适量浓氨水后生成蓝色沉淀,该沉淀溶于过量浓氨水中,溶液呈深蓝色Cu2++2OH-=Cu(OH)2↓ Cu(OH)2+4NH3·H2O=[Cu(NH3)4]2++2OH-+4H2O
Ag+①稀盐酸或可溶性盐酸盐②稀HNO3③氨水向未知溶液中加入稀盐酸再加入稀HNO3向过滤出的沉淀中加氨水生成白色沉淀,不溶于稀HNO3,但溶于氨水,生成[Ag(NH3)2]+Ag++Cl-=AgCl↓Ba2+稀H2SO4或可溶性酸盐溶液向未知溶液中加入稀H2SO4再加入稀HNO3产生白色沉淀,且沉淀不溶于稀HNO3Ba2++SO42-=BaSO4↓Fe3+KSCN溶液向未知溶液中加入KSCN溶液或加NaOH溶液或加苯酚变为血红色溶液Fe3++3SCN-=Fe(SCN)3加NaOH溶液产生红褐色沉淀Fe3++3OH-=Fe(OH)3↓加苯酚溶液显紫色Fe3++6C6H6OH→[Fe(C6H5O)]3-+6H+Fe2+①加NaOH溶液向未知溶液中加入NaOH溶液并露置在空气中开始时生成白色Fe(OH)2沉淀,迅速变成灰绿色,最后变成红褐色Fe(OH)3沉淀。Fe2++2OH-=Fe(OH)2↓ 4Fe(OH)2+O2+2H2O=4Fe(OH)3②KMnO4 (H+)溶液向未知溶液中加入KMnO4(H+)溶液KMnO4(H+)紫色褪去MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O③K3[Fe(CN)6]向未知溶液中加入K3[Fe(CN)6]溶液出现蓝色Fe3[Fe(CN)6]2沉淀3Fe2++2[Fe(CN)6]-=Fe3[Fe(CN)6]2↓④KSCN溶液,新制的氯水加入KSCN溶液,新制的氯水加入KSCN溶液不显红色,加入少量新制的氯水后,立即显红色。2Fe2++Cl2=2Fe3++2Cl-Fe3++3SCN-=Fe(SCN)3常见阴离子的检验方法:
离子检验试剂实验步骤实验现象离子方程式CO32-①BaCl2溶液、稀盐酸向未知溶液中加入BaCl2溶液再向沉淀中加入稀盐酸加入BaCl2溶液后生成白色沉淀,沉淀溶于稀盐酸,并放出无色无味气体Ba2++CO32-=BaCO3↓ BaCO3+2H+=Ba2++CO2↑+H2O②稀盐酸、Ca(OH)2溶液加入稀盐酸后放出的气体通入使澄清的Ca(OH)2溶液加入稀盐酸后放出无色无味气体,通入澄清的Ca(OH)2溶液变浑浊CO32-+2H+=H2O+CO2↑ Ca2++2OH-+CO2=CaCO3↓+H2OSO42-BaCl2溶液、稀硝酸或稀盐酸向未知溶液中加入BaCl2溶液再向沉淀中加入稀盐酸生成不溶于稀硝酸或稀盐酸的白色沉淀Ba2++SO42-=BaSO4↓SO32-①BaCl2溶液、稀盐酸向未知溶液中加入BaCl2溶液再向沉淀中加入稀盐酸加入BaCl2溶液后生成白色沉淀,沉淀溶于稀盐酸,并放出刺激性气味的气体SO32-+2H+=H2O+SO2↑②稀盐酸、品红溶液加入稀盐酸后放出的气体通入品红溶液加入稀盐酸后放出的气体使品红溶液褪色SO32-+2H+=H2O+SO2↑Cl-AgNO3溶液、稀硝酸或稀盐酸向未知溶液中加入AgNO3溶液,再向沉淀中加入稀盐酸生成不溶于稀硝酸或稀盐酸的白色沉淀Ag++Cl-=AgCl↓Br-AgNO3溶液、稀硝酸或稀盐酸生成不溶于稀硝酸或稀盐酸的浅黄色沉淀Ag++Br-=AgBr↓I-AgNO3溶液、稀硝酸或稀盐酸向未知溶液中加入AgNO3溶液,再向沉淀中加入稀盐酸生成不溶于稀硝酸的黄色沉淀Ag++I-=AgI↓②新制氯水,淀粉溶液向未知溶液中加入新制氯水,再加入淀粉溶液滴入新制Cl2,振荡后再滴入淀粉溶液,变蓝Ag++I-=AgI↓ 2I-+Cl2=I2+2Cl- I2遇淀粉变蓝注意: 1.若SO42-与Cl-同时检验,需注意检验顺序。应先用Ba(NO3)2溶液将SO42-检出,并滤去BaSO4,然后再用AgNO3检验Cl-。
2.检验SO32-的试剂中,只能用盐酸,不能用稀硝酸。因为稀硝酸能把SO32-氧化成SO42-。
3.若Ag+和Ba2+同时检验,也需注意检验顺序,应先用盐酸将Ag+检验出并滤去沉淀,然后再用稀硫酸检验Ba2+。




