题文
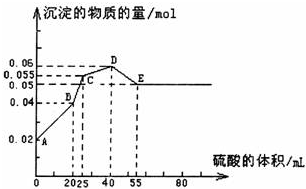
将由FeSO4、Ba(OH)2、AlCl3三种固体组成的混合物溶于足量的水中,用玻棒搅拌,充分溶解,一段时间后,向稳定的混合物溶液中滴加1mol•L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的物质的量关系如图所示.下列有关判断不正确的是( )A.AB段发生反应的离子方程式为:Ba2++SO42-+2H++2OH-=BaSO4↓+2H2OB.D点表示的溶液呈酸性C.C点表示的沉淀的化学式为Al(OH)3、BaSO4、Fe(OH)2D.混合物中FeSO4和AlCl3的物质的量相等
题型:未知 难度:其他题型
答案
由图可知最终沉淀0.05mol为BaSO4,由钡离子守恒可知,固体混合物中n[Ba(OH)2]=0.05mol,根据图象知,未加H2SO4前A点的沉淀为0.02mol,小于0.05mol,说明FeSO4完全反应,Ba2+有剩余.
由A→B一定发生反应Ba2++SO42-=BaSO4↓,加入20ml硫酸,硫酸的物质的量为0.02mol,由图可知沉淀量增加0.04mol-0.02mol=0.02mol,沉淀增加的物质的量等于加入的硫酸的物质的量,故不可能发生反应AlO2-+H++H2O=Al(OH)3↓,该反应硫酸的物质的量与沉淀的物质的量之比为1:2,也不会发生其它沉淀的溶解反应,否则沉淀量增加不可能为0.02mol,说明加入的20ml硫酸只与氢氧化钡反应.
故未加H2SO4前A点的溶液中Ba(OH)2有剩余,剩余三种固体组成的混合物溶于足量的水中,用玻璃棒搅拌,充分溶解,一段时间发生反应:FeSO4+Ba(OH)2=BaSO4↓+Fe(OH)2↓,4Fe(OH)2+2H2O+O2=4Fe(OH)3,Al3++4OH-=AlO2-+2H2O.故A点沉淀为Fe(OH)3、BaSO4,由方程式可知n[Fe(OH)3]=n(BaSO4)=0.01mol,此时Al3+变为AlO2-,可知原混合物固体中n(FeSO4)=0.01mol;
由B→C,加入5ml硫酸,硫酸的物质的量为0.005mol,由图可知沉淀量增加0.055mol-0.04mol=0.015mol,沉淀增加的物质的量等于加入的硫酸的物质的量的3倍,故发生反应Ba2++SO42-=BaSO4↓,AlO2-+H++H2O=Al(OH)3↓,由方程式可知,该阶段生成BaSO4为0.005mol,生成Al(OH)3为0.01mol.故C的沉淀为Fe(OH)3、BaSO4、Al(OH)3.
由C→D,加入15ml硫酸,硫酸的物质的量为0.015mol,由图可知沉淀量增加0.06mol-0.055mol=0.005mol,沉淀增加的物质的量等于加入的硫酸的物质的量的13倍,沉淀量达最大值,不可能单独发生Ba2++SO42-=BaSO4↓(沉淀增加的物质的量等于加入的硫酸的物质的量)或AlO2-+H++H2O=Al(OH)3↓(沉淀的物质的量是硫酸的2倍)或二者都发生;故该阶段发生反应Ba2++SO42-=BaSO4↓、Al(OH)3+3H+=Al3++3H2O、Fe(OH)3+3H+=Fe3++3H2O.说明C点AlO2-完全反应,D点的溶液含有Al3+、Fe3+.Ba2+沉淀完全.溶液为Al2(SO4)3、Fe2(SO4)3.
D→E发生反应Al(OH)3+3H+=Al3++3H2O、Fe(OH)3+3H+=Fe3++3H2O,E点完全溶解,溶液为Al2(SO4)3、Fe2(SO4)3.
由C→E共消耗30mLH2SO4,而0.01molFe(OH)3消耗15mLH2SO4,可知Al(OH)3消耗15mLH2SO4,判定n[Al(OH)3]=n[Fe(OH)3]=0.01mol,可知原混合固体中n(AlCl3)=0.01mol.
A、由上述分析可知,硫酸只与氢氧化钡反应,反应离子方程式为Ba2++SO42-+2H++2OH-=BaSO4↓+2H2O,故A正确;
B、由上述分析可知,D点的溶液含有Al3+、Fe3+,溶液为Al2(SO4)3、Fe2(SO4)3,Al3+、Fe3+水解,溶液呈酸性,故B正确;
C、由上述分析可知,C的沉淀为Fe(OH)3、BaSO4、Al(OH)3,故C错误;
D、由上述分析可知,原混合固体中n(FeSO4)=0.01mol,n(AlCl3)=0.01mol,故D正确.
故选:C.
解析
13
考点
据考高分专家说,试题“将由FeSO4、Ba(OH)2、AlCl.....”主要考查你对 [离子方程式 ]考点的理解。
离子方程式
离子方程式:
用实际参加反应的离子符号表示离子反应的式子。
离子方程式书写规则:
①写:写出化学反应方程式
②拆:把易溶于水、易电离的物质写成离子形式,难容难电离的物质及气体等仍用化学式表示
③删:删去方程式两边不参加反应的离子
④查:检查离子方程式两边各元素的原子个数和电荷总数是否相等
离子方程式书写及正误的判断方法:
①判断反应是否在水溶液中进行
因为电解质在水溶液中可以电离为自由移动的离子,在这种条件下才能发生离子反应。
②判断反应能否发生。
如果反应不能发生,当然也就没有离子方程式可言。
③判断反应物、生成物是否正确。
④判断质量和电荷是否守恒。
离子方程式不仅要质量守恒,而且反应前后各离子所带电荷总数必须相等。
⑤判断氧化物、难溶物、气体、单质、难电离的弱酸、弱碱、水是否写成了分子形式,而易电离的物质是否写成离子形式。
⑥判断连接符号“=”和“”及状态符号“↑”和“↓”运用是否正确。
强电解质的电离、不可逆反应、双水解反应用“=”;弱电解质电离、可逆反应、水解反应用“”。复分解反应、水解反应生成的难溶物用“↓”,气体用“↑”;单水解反应生成的难溶物不用“↓”,气体不用“↑”。
⑦判断微溶物的处理是否正确。
微溶物做反应物时,一般用离子形式,做生成物时一般用分子式。
⑧判断反应物的滴加顺序与方程式中生成物是否一致。
如:把碳酸钠溶液滴加到盐酸溶液中,和把盐酸滴加到碳酸钠溶液中反应产物是不同的。
⑨判断反应物的相对量与产物是否一致。
有些反应因反应物的量不同会生成不同的产物。如:CO2、SO2、H2S等气体与碱溶液反应时,若气体少量,则生成正盐;若气体过量,则生成酸式盐。
⑩判断电解质在写成离子形式时阴阳离子个数比是否合理。
如Ba(OH)2溶液和稀H2SO4反应的离子方程式往往错误写成: ,正确为:
书写与量有关的离子方程式:
基本方法是:把物质的量少的物质的系数定为1,其他物质按最大量消耗。
1.因滴加顺序不同造成连续反应
- HCl与Na2CO3
向Na2CO3溶液中滴入盐酸溶液至过量,其离子反应分步写 (1)CO32-+H+==HCO3- (2)HCO3-+H+==CO2↑+H2O
若向盐酸溶液中滴入Na2CO3溶液至不再产生气体,其离子反应一步完成 CO32-+2H+==CO2↑+H2O
若向足量Na2CO3溶液中加入少量的盐酸溶液,其离子方程式为: CO32-+H+==HCO3-
- HCl与NaAlO2
向Na2CO3溶液中滴入盐酸溶液至过量,其离子反应分步写 (1)CO32-+H+==HCO3- (2)HCO3-+H+==CO2↑+H2O
若向盐酸溶液中滴入Na2CO3溶液至不再产生气体,其离子反应一步完成 CO32-+2H+==CO2↑+H2O
若向足量Na2CO3溶液中加入少量的盐酸溶液,其离子方程式为: CO32-+H+==HCO3-
- AlCl3与NaOH
向AlCl3溶液中滴入NaOH溶液至过量,其离子反应分步写 (1)Al3++3OH-==Al(OH)3↓ (2)Al(OH)3+OH-==AlO2-+2H2O
若向NaOH溶液中加入少量AlCl3溶液,其离子反应一步完成 Al3++4OH-==AlO2-+2H2O
若向足量Al2(SO4)3溶液中加入少量的NaOH溶液,其离子方程式为: Al3++3OH-==Al(OH)3↓
- AgNO3与NH3·H2O
向AgNO3溶液中滴入稀NH3·H2O至过量,其离子反应分步写(1) Ag++NH3·H2O==AgOH↓+NH4+ (2)AgOH+2NH3·H2O==Ag(NH3)2++OH-+2H2O
若向NH3·H2O溶液中加入少量AgNO3,其离子反应一步完成 Ag++3NH3·H2O==Ag(NH3)2++OH-+NH4++2H2O
若向足量AgNO3溶液中滴入少量NH3·H2O,其离子方程式为:Ag++NH3·H2O==AgOH↓+NH4+
- CO2与NaOH
向NaOH溶液中通人CO2气体至过量,其离子反应分步写 (1)2OH-+CO2==CO32-+H2O (2)CO32-+CO2+H2O==2HCO3-
若向足量NaOH溶液中通人少量CO2气体,其离子方程式为: 2OH-+CO2==CO32-+H2O
若向NaOH溶液中通人过量CO2气体,其离子反应一步完成 OH-+CO2==HCO3-
2.过量型:
向足量的Ca(HCO3)2溶液中逐渐滴入NaOH溶液 OH-+Ca2++HCO3-==H2O+CaCO3↓
向足量的NaOH溶液中逐渐滴入Ca(HCO3)2溶液 Ca2++2HCO3-+2OH-==2H2O+CaCO3↓+CO32-
Fe与HNO3 :铁过量时:Fe+4HNO3==Fe(NO3)3+NO↑+2H2O
铁不足时:3Fe+8HNO3==3Fe(NO3)2+2NO↑+4H2O
3.定量型:
因还原性I->Fe2+>Br-,所以在FeI2或者FeBr2中通入一定量的Cl2,发生不同的离子反应,依次为:
(1)2I-+Cl2==2Cl-+I2(2)2Fe2++Cl2==2Fe3++2Cl-(3)2Br-+Cl2==2Cl-+Br2
4.目标型
向明矾溶液逐滴滴加Ba(OH)2溶液至硫酸根离子刚好沉淀完全 Al3++SO42-+Ba2++4OH-==AlO2-+2BaSO4↓+2H2O
向明矾溶液逐滴滴加Ba(OH)2溶液至铝离子刚好沉淀完全 Al3+SO42-+Ba2++3OH-==Al(OH)3↓+2BaSO4↓
null
null
null
null
null