题文
Ⅰ.化合物A、B是中学常见的物质,其阴阳离子可从下表中选择阳离子 K+ Na+ Fe2+ Ba2+ NH4+ 阴离子 OH- NO3- I- HSO3- AlO2- HSO4-
(1)若A、B的水溶液均为无色,B的水溶液呈碱性,且混合后只产生不溶于稀硝酸的白色沉淀及能使红色石蕊试纸变蓝的气体。
①B的化学式为___________;
②A、B溶液混合后加热呈中性反应的离子方程式为_____________。
(2)若A的水溶液呈浅绿色,B的水溶液无色且其焰色反应为黄色。向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合亦无明显变化。则
①A为__________;B为___________;
②经分析上述过程中溶液变黄的原因可能是有两种:Ⅰ______________ Ⅱ ___________;
③请用一简易方法证明上述溶液变黄的原因 ______________;
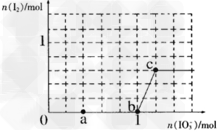
Ⅱ.已知溶液中,还原性:HSO3->I-,氧化性:IO3->I2>SO42-。在含3mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,据图回答下列问题:
(2)当n(I2)达最大时,n(IO3-)对应的最小值为__________mol,此时反应的离子方程式是_________________。
题型:未知 难度:其他题型
答案
Ⅰ.(1)① Ba(OH)2
②H+ +SO42-+ NH4+ + Ba2+ +2OH- ===BaSO4↓+ NH3↑+ 2H2O
(2)①FeI2 ; NaNO3
② Ⅰ 仅有Iˉ被氧化成I2使溶液呈黄色; Ⅱ I-、Fe2+均被氧化使溶液呈黄色
③ 取少量变黄溶液于试管中,滴加几滴KSCN溶液,若变红则Ⅱ合理(其他合理亦可
Ⅱ. (1)SO42- , 3HSO3-+ IO3-=== 3SO42- + I-+ 3 H+
(2)1.2mol,5Iˉ+ IO3-+ 6 H+ === 3I2 + 3H2O
解析
该题暂无解析
考点
据考高分专家说,试题“Ⅰ.化合物A、B是中学常见的.....”主要考查你对 [氧化还原反应的计算 ]考点的理解。
氧化还原反应的计算
氧化还原反应的计算:
(1)比较典型的计算有:求氧化剂、还原剂物质的量之比或质量比,计算参加反应的氧化剂货还原剂的量,确定反应前后某一元素的价态变化等。
(2)计算的依据是:氧化剂得电子数等于还原剂失电子数,列出守恒关系式求解。
氧化还原反应的基本规律:
1.守恒规律
氧化还原反应中有物质失电子必有物质得电子,且失电子总数等于得电子总数。或者说氧化还原反应中,有元素化合价升高必有元素化合价降低,且化合价升高总数必等于降低总数。有关得失电子守恒(化合价守恒)的规律有如下应用:
(1)求某一反应中被氧化与被还原的元素原子个数之比,或求氧化剂与还原剂的物质的量之比及氧化产物与还原产物的物质的量之比。
(2)配平氧化还原反应方程式。
(3)进行有关氧化还原反应的计算:
2.强弱规律
较强氧化性的氧化剂跟较强还原性的还原剂反应,生成弱还原性的还原产物和弱氧化性的氧化产物。应用:在适宜条件下,用氧化性较强的物质制备氧化性较弱的物质,或用还原性较强的物质制备还原性较弱的物质,也可用于比较物质间氧化性或还原性的强弱。
3.价态规律
元素处于最高价,只有氧化性;元素处于最低价,只有还原性;元素处于中间价态,既有氧化性又有还原性,但主要表现一种性质。物质若含有多种元素,其性质是这些元素性质的综合体现。
4.转化规律
氧化还原反应中,以元素相邻价态之间的转化最容易;不同价态的同种元素之间发生反应,元素的化合价只靠近,不交叉;相邻价态的同种元素之间不发生氧化还原反应。如
5.难易规律
越易失去电子的物质,失去后就越难得到电子;越易得到电子的物质,得到后就越难失去电子。一种氧化剂同时和几种还原剂相遇时,还原性最强的优先发生反应;同理,一种还原剂同时与多种氧化剂相遇时,氧化性最强的优先发生反应,如向FeBr2溶液中通入Cl2时,发生离子反应的先后顺序为:。