题文
下列制取单质的反应中,化合物作还原剂的是( )A.Fe+H2SO4====FeSO4+H2↑B.Br2+2NaI====2NaBr+I2C.2C+SiO2
Si+2CO↑D.2Al+Fe2O3
2Fe+Al2O3
题型:未知 难度:其他题型
答案
B
解析
还原剂在反应中失电子,化合价升高。逐项分析所给反应的化合物中各元素的化合价变化,只有B中碘元素的化合价由-1价升到0价,失电子,KI作还原剂。也可根据所给反应都是一种单质和一种化合物的反应,其中A、C、D 3项中的单质都是元素化合价升高失电子的变化,这些单质肯定是还原剂,与它们反应的化合物一定是氧化剂。B是单质,化合价降低,得电子,单质是氧化剂,与之反应的化合物必是还原剂。
考点
据考高分专家说,试题“下列制取单质的反应中,化合物作还原剂的是.....”主要考查你对 [氧化还原反应与基本反应类型的关系 ]考点的理解。
氧化还原反应与基本反应类型的关系
氧化还原反应与基本反应类型的关系:
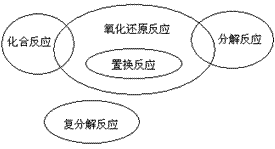
化合反应有单质参加的是氧化还原反应;分解反应有单质生成的是氧化还原反应;置换反应全部是氧化还原反应;复分解反应都是非氧化还原反应
化学反应的分类:
化学反应按照不同的分类标准,可以分成不同的反应类型
- 根据原子(原子团)的组合形式来分类,把化学反应分为化合反应、分解反应、置换反应、复分解反应,
但是四种基本类型的反应并不能包括所有的化学反应,比如3O2==2O3。 - 按是否有电子转移,把化学反应分为氧化还原反应和非氧化还原反应。
- 按是否有离子参加反应,把化学反应分为离子反应和非离子反应。
- 按化学反应的能量关系,把化学反应分为放热反应和吸热反应。
- ……
null
null
null
null
null