题文
已知下列变化中,0.2 mol x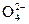
参加反应时共转移0.4 mol电子,
Rx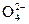
+
+ H+——RO2+ Mn2++H2O
(1)求x的值。
(2)求参加反应的H+的物质的量。
题型:未知 难度:其他题型
答案
(1)2 (2)0.64 mol
解析

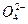

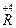
O2
1 mol Rx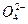
转化为RO2失去电子的物质的量为:(4-
)x,即(4x-6) mol
所以(4x-6)×0.2 mol="0.4" mol,解得:x=2。
配平后的该反应方程式为:
5R2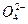
+2Mn
+16H+====10RO2+2Mn2++8H2O
参加反应的H+为:n(H+)=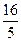
·n(R2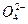
)=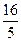
×0.2 mol="0.64" mol
考点
据考高分专家说,试题“已知下列变化中,0.2 mol x参加反.....”主要考查你对 [氧化还原反应与基本反应类型的关系 ]考点的理解。
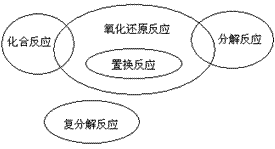
氧化还原反应与基本反应类型的关系
氧化还原反应与基本反应类型的关系:
化合反应有单质参加的是氧化还原反应;分解反应有单质生成的是氧化还原反应;置换反应全部是氧化还原反应;复分解反应都是非氧化还原反应
化学反应的分类:
化学反应按照不同的分类标准,可以分成不同的反应类型
- 根据原子(原子团)的组合形式来分类,把化学反应分为化合反应、分解反应、置换反应、复分解反应,
但是四种基本类型的反应并不能包括所有的化学反应,比如3O2==2O3。 - 按是否有电子转移,把化学反应分为氧化还原反应和非氧化还原反应。
- 按是否有离子参加反应,把化学反应分为离子反应和非离子反应。
- 按化学反应的能量关系,把化学反应分为放热反应和吸热反应。
- ……
null
null
null
null
null