题文
(11分)回答下列问题
(1)在2FeBr2+3Cl2=2FeCl3+2Br2的反应中,被氧化的元素是_____________
(2)铁钉在氯气中被锈蚀成棕褐色物质FeCl3,而在盐酸中生成淡绿色溶液(FeCl2);浓盐酸中滴加KMnO4溶液产生黄绿色气体(Cl2)。则Cl2、Fe3+、MnO4-氧化性由强到弱的顺序是____________________。
(3)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式____________________________________________。
(4)在一定条件下,RO3n-和Cl2可发生如下反应:RO3n-+Cl2+2OH-=RO42-+2Cl-+H2O
由以上反应可知在上述过程中RO3n-被________________(填“氧化”或“还原”),RO3n-中元素R的化合价是______________。
题型:未知 难度:其他题型
答案
(11分)(1)Fe(2分)和Br(2分) (2)MnO4->Cl2>Fe3+ (2分)
(3)3CuO+2NH3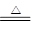
3Cu+N2+3H2O(2分)(4)氧化(1分) +4(2分)
解析
(1)根据反应的方程式可知,溴化铁中铁元素的化合价从+2价升高到+3价,被氧化。而溴元素的化合价溴-1价升高到0价,被氧化。
(2)在氧化还原反应中氧化剂的氧化性强于氧化产物的,所以反应中的实验现象可判断,Cl2、Fe3+、MnO4-氧化性由强到弱的顺序是MnO4->Cl2>Fe3+。
(3)因为氧化铜具有氧化性,所以根据原子守恒可知,两种单质应该是氮气和铜,则反应的化学方程式是3CuO+2NH3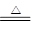
3Cu+N2+3H2O。
(4)氯元素的化合价降低,所以氯气是氧化剂,则RO3n-被氧化,作还原剂。RO42-中R元素的化合价是+6价,所以根据电子的得失守恒可知,RO3n-中元素R的化合价是+(6-2)=+4价。
点评:该题是中等难度的试题,试题基础性强,侧重能力的培养。该题的关键是准确标出有关元素的化合价变化情况,然后根据氧化还原反应的有关概念灵活运用、计算判断即可。
考点
据考高分专家说,试题“(11分)回答下列问题(1)在2FeBr.....”主要考查你对 [氧化还原反应与基本反应类型的关系 ]考点的理解。
氧化还原反应与基本反应类型的关系
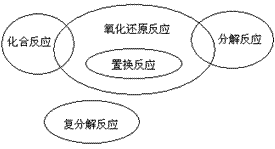
氧化还原反应与基本反应类型的关系:
化合反应有单质参加的是氧化还原反应;分解反应有单质生成的是氧化还原反应;置换反应全部是氧化还原反应;复分解反应都是非氧化还原反应
化学反应的分类:
化学反应按照不同的分类标准,可以分成不同的反应类型
- 根据原子(原子团)的组合形式来分类,把化学反应分为化合反应、分解反应、置换反应、复分解反应,
但是四种基本类型的反应并不能包括所有的化学反应,比如3O2==2O3。 - 按是否有电子转移,把化学反应分为氧化还原反应和非氧化还原反应。
- 按是否有离子参加反应,把化学反应分为离子反应和非离子反应。
- 按化学反应的能量关系,把化学反应分为放热反应和吸热反应。
- ……
null
null
null
null
null