题文
(10分)铁元素的化合价有+2、+3两种,磁铁矿的主要成分是Fe3O4,能与盐酸反应生成两种盐。
(1)请用铁的+2价、+3价的氧化物形式表示Fe3O4可写成___________________
(2)写出Fe3O4与盐酸反应的离子方程式_________________。
(3)设计实验验证反应后溶液中含有Fe3+所用的试剂和反应的化学方程式__________、______________。
(4)设计实验验证反应后溶液中不含Fe3+而可能含有Fe2+。进行实验操作的顺序有:①加入足量氯水,②加入足量高锰酸钾溶液,③加入少量硫氰化钾溶液,选择所需要的试剂及先后的顺序是______________(注意先后顺序)。
(5)将反应后的溶液中Fe3+全部转化为Fe2+,最适宜的物质是选用___________。
(6)将反应后的溶液中Fe2+全部转化为Fe3+,选用的绿色试剂是H2O2 ,H2O2在酸性的条件下将Fe2+氧化为Fe3+,写出反应的离子方程式___________________。
题型:未知 难度:其他题型
答案
(10分) (1)FeO·Fe2O3 (1分) (2)Fe3O4+8H+=2Fe3++Fe2++4H2O (2分)
(3)KSCN (1分) FeCl3+3KSCN=Fe(SCN)3+3KCl (2分)
(4) ③① (1分) (5)铁 (1分)
(6)2Fe2++H2O2+2H+=2Fe3++2H2O (2分)
解析
(1)设四氧化三铁中+2价、+3价的铁分别是a和b,则a+b=3、2a+3b=4×2,解得x=1、b=2,所以铁的+2价、+3价的氧化物形式表示Fe3O4可写成FeO·Fe2O3。
(2)根据(1)可知,Fe3O4与盐酸反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O。
(3)铁离子能和KSCN溶液反应使溶液显红色,所以验证反应后溶液中含有铁离子的试剂使KSCN溶液,反应的化学方程式是FeCl3+3KSCN=Fe(SCN)3+3KCl。
(4)验证反应后溶液中不含Fe3+而可能含有Fe2+,则首先应该加入KSCN溶液,如果不变色,再加入氧化剂。由于酸性高锰酸钾溶液是紫红色,所以选择的氧化剂最好是新制的氯水,答案是③①。
(5)铁离子能把铁氧化生成亚铁离子,而铁离子也是被还原生成亚铁离子,所以将反应后的溶液中Fe3+全部转化为Fe2+,最适宜的物质是选用铁。
(6)双氧水的还原产物是水,则反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O。
点评:该题是中等难度的试题,试题综合性强,考查的知识点比较多。该题再注重对性质基础知识考查和巩固的图示,主要是侧重培养学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑思维能力和创新思维能力。
考点
据考高分专家说,试题“(10分)铁元素的化合价有+2、+3两种.....”主要考查你对 [氧化还原反应与基本反应类型的关系 ]考点的理解。
氧化还原反应与基本反应类型的关系
氧化还原反应与基本反应类型的关系:
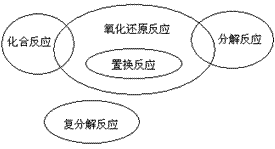
化合反应有单质参加的是氧化还原反应;分解反应有单质生成的是氧化还原反应;置换反应全部是氧化还原反应;复分解反应都是非氧化还原反应
化学反应的分类:
化学反应按照不同的分类标准,可以分成不同的反应类型
- 根据原子(原子团)的组合形式来分类,把化学反应分为化合反应、分解反应、置换反应、复分解反应,
但是四种基本类型的反应并不能包括所有的化学反应,比如3O2==2O3。 - 按是否有电子转移,把化学反应分为氧化还原反应和非氧化还原反应。
- 按是否有离子参加反应,把化学反应分为离子反应和非离子反应。
- 按化学反应的能量关系,把化学反应分为放热反应和吸热反应。
- ……
null
null
null
null
null