题文
研究NO2、SO2、CO等大气污染气体的处理以及燃料的开发与利用有重要意义。
(1)NO2可用水吸收,利用反应6NO2+8NH3
7N2+12H2O
也可以处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是______________L。
(2)已知:2SO2(g)+ O2 (g)
2SO3 (g) △H =-196.6kJ·mol-1
2NO(g)+ O2 (g) 
2NO2 (g) △H =-113.0kJ·mol-1
则反应NO2(g)+ SO2 (g) 
SO3 (g) +NO(g)的△H =______kJ·mol-1
(3)CO可用于合成甲醇,反应方程式为CO(g)+ 2H2 (g) 
CH3OH (g)。由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量是现用镍氢电池和锂电池的10倍,可连续使用1个月充电一次。假定放电过程中,甲醇完全氧化产生的CO2被充分吸收生成CO32-
①该电池反应的总离子方程式为____________________________________________。
②甲醇在____极发生反应(填正或负),电池在放电过程中溶液的pH将____________(填降低或上升、不变);若有16克甲醇蒸气被完全氧化,产生的电能电解足量的CuSO4溶液,(假设整个过程中能量利用率为80%),则将产生标准状况下的O2________________升。
题型:未知 难度:其他题型
答案
(16分每空二分)(1)6.72 (2)-41.8;
(3)2CH3OH+3O2+4OH-=2CO32-+6H2O 负 下降 13.44
解析
(1)在反应6NO+8NH3
7N5+12 H2O中NO2作氧化剂,化合价由反应前的+4价降低到反应后0价,因此当反应中转移1.2mol电子时,消耗NO2的物质的量为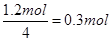
,所以标准状况下的体积是
。
(2)根据热化学方程式① 2SO2(g)+O2(g)
2SO3(g) ΔH1=-196.6 kJ·mol-1 、② 2NO(g)+O2(g)
2NO2(g) ΔH2=-113.0 kJ·mol-1可知,(②-①)÷2即得出NO2(g)+SO2(g)
SO3(g)+NO(g) ΔH=(ΔH2-ΔH1)÷2=(-113.0 kJ/mol+196.6 kJ/mol)÷2=+41.8kJ/mol。
(3)①由于电解质是强碱溶液,所以该甲醇燃料电池的总反应式是2CH3OH+3O2+4OH-=2CO32-+6H2O。
②原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应,所以甲醇在负极通入。根据总反应式可知,电池在放电过程中溶液的pH将减小。16g甲醇的物质的量是16g÷32g/mol=0.5mol,在反应中失去0.5mol×6=3mol电子,则根据电子的得失守恒可知,生成氧气的物质的量是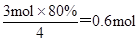
,则氧气在标准状况下的体积是0.6mol×22.4L/mol=13.44L。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,贴近高考,旨在培养学生灵活运用基础知识解决实际问题的能力的培养,有利于调动学生的学习兴趣,激发学生的学习积极性,提高学生的应试能力和学习效率。
考点
据考高分专家说,试题“研究NO2、SO2、CO等大气污染气体的.....”主要考查你对 [氧化还原反应与基本反应类型的关系 ]考点的理解。
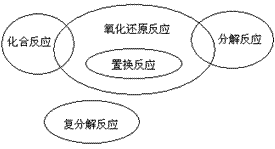
氧化还原反应与基本反应类型的关系
氧化还原反应与基本反应类型的关系:
化合反应有单质参加的是氧化还原反应;分解反应有单质生成的是氧化还原反应;置换反应全部是氧化还原反应;复分解反应都是非氧化还原反应
化学反应的分类:
化学反应按照不同的分类标准,可以分成不同的反应类型
- 根据原子(原子团)的组合形式来分类,把化学反应分为化合反应、分解反应、置换反应、复分解反应,
但是四种基本类型的反应并不能包括所有的化学反应,比如3O2==2O3。 - 按是否有电子转移,把化学反应分为氧化还原反应和非氧化还原反应。
- 按是否有离子参加反应,把化学反应分为离子反应和非离子反应。
- 按化学反应的能量关系,把化学反应分为放热反应和吸热反应。
- ……
null
null
null
null
null