题文
美国科学家理查德·海克和日本科学家根岸英一、伶木彰因在研发“有机合成中的钯催化的交叉偶联”而获得诺贝尔化学奖。有机合成常用的钯/活性炭催化剂,长期使用催化剂会被杂质(如:铁、有机物等)污染而失去活性,成为废催化剂,需对其再生回收,一种由废催化剂制取氯化钯的工艺流程如下:
(1)甲酸还原氧化钯的化学方程式为 。
(2)钯在王水(浓硝酸与浓盐酸按体积比1:3)中转化为H2PdC14,硝酸被还原为NO,该反应的化学方程式为: 。
(3)钯精渣中钯的回收率高低主要取决于王水溶解的操作条件,已知反应温度、反应时间和王水用量对钯回收率的影响如下图1—图3所示,则王水溶液钯精渣的适宜条件(温度、时间和王水用量)为 、 、 。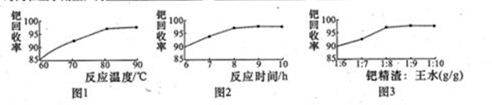
(4)加浓氨水时,钯转变为可溶性[Pd(NH3)4]2—。此时铁的存在形式是 (写化学式)
(5)700℃焙烧1的目的是: ;550℃焙烧2的目的是: 。
题型:未知 难度:其他题型
答案
(15分)(1)PdO+HCOOH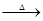
Pd+CO2↑+H2O(3分)
(2)3Pd+12HCl+2HNO3=3H2PdCl4+2NO↑+4H2O(3分)
(3)80~90℃(或90℃左右)、反应时间约为8h、钯精渣与王水的质量比为1:8(3分)
(4)Fe(OH)3(2分)
(5)除去活性炭及有机物(2分);脱氨(将Pd(NH3)2Cl2转变为PdCl2)(2分)
解析
(1)氧化钯的还原产物是Pd,而甲酸的氧化产物是CO2,所以甲酸还原氧化钯的化学方程式为)PdO+HCOOH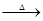
Pd+CO2↑+H2O。
(2)根据原子守恒可知,反应中还有水生成,因此反应的化学方程式是3Pd+12HCl+2HNO3=3H2PdCl4+2NO↑+4H2O。
(3)根据图1可知,80~90℃回收率最高。根据图2可知,反应进行到8h后,回收率几乎不再发生变化。根据图3可知,钯精渣与王水的质量比为1:8是回收率最高,所以王水溶液钯精渣的适宜条件是80~90℃(或90℃左右)、反应时间约为8h、钯精渣与王水的质量比为1:8。
(4)氨水溶液显碱性,所以铁的主要存在形式是Fe(OH)3。
(5)由于催化剂中含有活性炭以及有机物,所以700℃焙烧1的目的是除去活性炭及有机物;由于要把Pd(NH3)2Cl2转变为PdCl2,所以550℃焙烧2的目的是脱氨(将Pd(NH3)2Cl2转变为PdCl2)。
考点
据考高分专家说,试题“美国科学家理查德·海克和日本科学家根岸英.....”主要考查你对 [氧化还原反应与基本反应类型的关系 ]考点的理解。
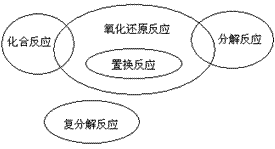
氧化还原反应与基本反应类型的关系
氧化还原反应与基本反应类型的关系:
化合反应有单质参加的是氧化还原反应;分解反应有单质生成的是氧化还原反应;置换反应全部是氧化还原反应;复分解反应都是非氧化还原反应
化学反应的分类:
化学反应按照不同的分类标准,可以分成不同的反应类型
- 根据原子(原子团)的组合形式来分类,把化学反应分为化合反应、分解反应、置换反应、复分解反应,
但是四种基本类型的反应并不能包括所有的化学反应,比如3O2==2O3。 - 按是否有电子转移,把化学反应分为氧化还原反应和非氧化还原反应。
- 按是否有离子参加反应,把化学反应分为离子反应和非离子反应。
- 按化学反应的能量关系,把化学反应分为放热反应和吸热反应。
- ……
null
null
null
null
null