题文
高锰酸钾(KMnO4)是一种常用的氧化剂。
I.(1)有下列变化: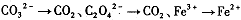
,找出其中一个变化与“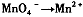
”组成一个反应,写出该反应的离子方程式____ 。
(2)不同条件下高锰酸钾可发生如下反应:

由此可知,高锰酸根离子(MnO—4)反应后的产物与 有关。
(3)高锰酸钾溶液与硫化亚铁有如下反应:
若上述反应前后固体的质量减少了2.8g,则硫元素与KMnO4之间发生电子转移的数目为 个。
Ⅱ.酒后驾车已成为一个社会问题。检测驾驶人员呼气中酒精浓度(BrAC)的方法有多种。
(4)早期是利用检测试剂颜色变化定性判断BrAC,曾用如下反应检测BrAC:
完成并配平上述反应。
(5)受上述方法启发,后来用五氧化二碘的淀粉溶液检测BrAC,乙醇被氧化为乙醛,该反应的化学方程式为____ 。
题型:未知 难度:其他题型
答案
14分
⑴2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O (3分)
⑵溶液酸碱性 (2分)
⑶0.1NA (6.02×1022) (3分)
⑷3CH3CH2OH+2KMnO4=3CH3CHO+2MnO2+2KOH+2H2O (3分)
⑸I2O5+5 CH3CH2OH→I2+5CH3CHO+5H2O (3分)
解析
⑴“MnO4-→Mn2+”是还原,那么另一过程必定是氧化,故只有“C2O42-→CO2”合题意,方程式为2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O。
⑵由条件中的三个半反应可知是溶液酸碱性。
⑶由化学方程式可得关系式:10FeS ~ 10S ~ Δm(固)~ 转移e-
880g 320g 560g 20mol
2.8g ∴0.1mol
转移电子数目为0.1NA (或6.02×1022)。
⑷由于反应生成了碱,根据第⑵题可知KMnO4被还原为MnO2,故方程式为:
3CH3CH2OH+2KMnO4=3CH3CHO+2MnO2+2KOH+2H2O
⑸用五氧化二碘的淀粉溶液检测BrAC,乙醇被氧化为乙醛,那么I2O5就被还原为I2。
I2O5+5 CH3CH2OH→I2+5CH3CHO+5H2O
考点
据考高分专家说,试题“高锰酸钾(KMnO4)是一种常用的氧化剂.....”主要考查你对 [氧化还原反应与基本反应类型的关系 ]考点的理解。
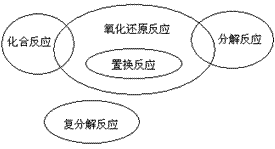
氧化还原反应与基本反应类型的关系
氧化还原反应与基本反应类型的关系:
化合反应有单质参加的是氧化还原反应;分解反应有单质生成的是氧化还原反应;置换反应全部是氧化还原反应;复分解反应都是非氧化还原反应
化学反应的分类:
化学反应按照不同的分类标准,可以分成不同的反应类型
- 根据原子(原子团)的组合形式来分类,把化学反应分为化合反应、分解反应、置换反应、复分解反应,
但是四种基本类型的反应并不能包括所有的化学反应,比如3O2==2O3。 - 按是否有电子转移,把化学反应分为氧化还原反应和非氧化还原反应。
- 按是否有离子参加反应,把化学反应分为离子反应和非离子反应。
- 按化学反应的能量关系,把化学反应分为放热反应和吸热反应。
- ……
null
null
null
null
null