题文
高锰酸钾可用于除去地下水的硫化氢异味的原理是生成的硫和二氧化锰等沉淀物可过滤除去。水体呈弱酸性时,高锰酸钾的还原产物是MnO和MnO2,且MnO和MnO2的物质的量比为3:1。
(1)写出并配平上述化学方程式,标出电子转移方向与数目。
KMnO4 + H2S +H2SO4 →
在处理饮用水时,活性炭应在高锰酸钾反应结束后投加,否则会发生反应:
KMnO4 + C +H2O →MnO2 + X +K2CO3 (未配平)
(2)X的化学式为__________。
(3) 1mol氧化剂被______(填“氧化”或“还原”)时,生成_____mol氧化产物
题型:未知 难度:其他题型
答案
(1)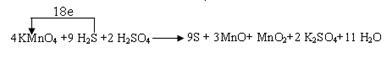
(4分)
(2)KHCO3 (2分)
(3)还原 ,0.75 (各1分,共2分)
解析
(1)由题目信息可知,KMnO4、H2S、H2SO4反应生成S、MnO、MnO2,同时还生成K2SO4、H2O,生成MnO和MnO2的物质的量比为3:1。其中Mn元素的 化合价从+7价降低+2价和+4价,S元素的化合价从-2价升高到0价,设MnO和MnO2的系数分别为为3、1,则根据电子转移守恒可知S的系数为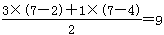
。根据原子守恒可知,KMnO4系数为4,H2S系数为9,K2SO4的系数为2,H2SO4的系数为2,H2O的系数为11,因此配平后方程式为:4KMnO4+9H2S+2H2SO4=9S+3MnO+MnO2+2K2SO4+11H2O,则反应中转移电子数目为9×[0-(-2)]=18,所以标出电子转移方向与数目为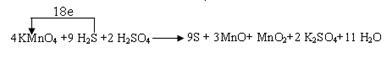
。
(2)反应中KMnO4→Mn02,Mn元素化合价由+7价降低为+4价,得到3个电子。C→K2CO3,C元素化合价由0价升高为+4价,失去4个电子。所以化合价升降最小公倍数为12,故KMnO4系数为4,C的系数为3,由C、K的原子数目关系可知K2CO3系数为1,因此X含有+4价的C原子、且C原子与K原子之比为1:1,所以X为KHCO3。
(3)反应中KMn04是氧化剂被还原,发生还原反应。氧化产物为KHCO3、K2CO3,每摩尔KHCO3、K2CO3都含1molC原子,设生成的氧化产物为amol,则根据电子转移守恒可知1mol×(7-4)=amol×(4-0),解得a=0.75。
考点
据考高分专家说,试题“高锰酸钾可用于除去地下水的硫化氢异味的原.....”主要考查你对 [氧化还原反应与基本反应类型的关系 ]考点的理解。
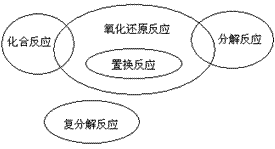
氧化还原反应与基本反应类型的关系
氧化还原反应与基本反应类型的关系:
化合反应有单质参加的是氧化还原反应;分解反应有单质生成的是氧化还原反应;置换反应全部是氧化还原反应;复分解反应都是非氧化还原反应
化学反应的分类:
化学反应按照不同的分类标准,可以分成不同的反应类型
- 根据原子(原子团)的组合形式来分类,把化学反应分为化合反应、分解反应、置换反应、复分解反应,
但是四种基本类型的反应并不能包括所有的化学反应,比如3O2==2O3。 - 按是否有电子转移,把化学反应分为氧化还原反应和非氧化还原反应。
- 按是否有离子参加反应,把化学反应分为离子反应和非离子反应。
- 按化学反应的能量关系,把化学反应分为放热反应和吸热反应。
- ……
null
null
null
null
null