题文
碘化亚铜(Cu2I2)是一种不溶于水也不溶于酸的白色固体,用途很广泛。
完成下列填空:
(1)碘化钾溶液中滴加适量硫酸铜溶液,就能得到碘化亚铜。请完成并配平上述反应:
____KI+____CuSO4 → ____I2+____Cu2I2↓+ ____________
该反应中氧化剂与还原剂的物质的量之比为___________。
(2)往上述反应后溶液中加入淀粉,溶液变蓝,再滴加亚硫酸溶液,蓝色又褪去。
写出KI、Cu2I2、H2SO3的还原性由强到弱的顺序是____________________。
(3)碘化亚铜能用于检测空气中的汞蒸气,其反应为:
2Cu2I2+Hg → Cu2HgI4(玫瑰红)+ 2Cu
产物Cu2HgI4中,Cu元素显____价。
当有1 molCu2I2参与反应时,转移电子____mol。
(4)为除去稀盐酸中少量CuCl2杂质,可往溶液中加入过量的M试剂后进行过滤操作,再通入适量的Cl2后进行N操作。试剂M和操作N的组合正确的是_____(选填编号)
选项
试剂M
操作N
a
碘化钾溶液
升华
b
氢碘酸溶液
萃取分液
c
氢气
过滤
d
氢硫酸溶液
过滤
题型:未知 难度:其他题型
答案
(1)4、2、1、1、2K2SO4(2分);1:1(1分)
(2)H2SO3、KI、Cu2I2(1分)
(3)+1(1分);1(1分)
(4)bd(2分)
解析
(1)缺项配平,先根据电子守恒配平,后根据原子守恒配平,4KI+2CuSO4=I2+Cu2I2↓+2K2SO4, 4molKI中2mol为氧化剂生成碘单质,2mol不作为氧化剂生成 Cu2I2,故答案为2:2=1:1;
(2)根据氧化剂的氧化性强于氧化产物,还原剂的还原性强于还原产物判断,H2SO3、KI、Cu2I2;
(3)根据该物质中碘元素为-1价,汞元素为+1或+2价,根据化合价为零原则,判断该物质中汞元素为+2价,铜元素为+1价,根据方程式判断该反应中电子转移为2个,故当有1 molCu2I2参与反应时,转移电子1mol;
(4)a、加入碘化钾处理后再通入氯气,把过量的碘化钾除去生成碘单质,但溶液中碘单质只能用萃取分液的方法除去,错误;b、正确;c、错误;d、氢硫酸与硫酸铜反应生成不溶于酸的硫化铜沉淀,后铜与氯气与过量的氢硫酸反应生成盐酸和硫沉淀,过滤除去,正确。
考点
据考高分专家说,试题“碘化亚铜(Cu2I2)是一种不溶于水也不.....”主要考查你对 [氧化还原反应与基本反应类型的关系 ]考点的理解。
氧化还原反应与基本反应类型的关系
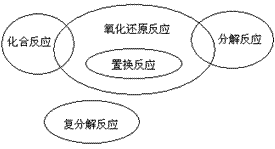
氧化还原反应与基本反应类型的关系:
化合反应有单质参加的是氧化还原反应;分解反应有单质生成的是氧化还原反应;置换反应全部是氧化还原反应;复分解反应都是非氧化还原反应
化学反应的分类:
化学反应按照不同的分类标准,可以分成不同的反应类型
- 根据原子(原子团)的组合形式来分类,把化学反应分为化合反应、分解反应、置换反应、复分解反应,
但是四种基本类型的反应并不能包括所有的化学反应,比如3O2==2O3。 - 按是否有电子转移,把化学反应分为氧化还原反应和非氧化还原反应。
- 按是否有离子参加反应,把化学反应分为离子反应和非离子反应。
- 按化学反应的能量关系,把化学反应分为放热反应和吸热反应。
- ……
null
null
null
null
null