题文
在5.6 g Fe粉中加入过量的稀硫酸溶液,待反应完全后,再加入1mol·L-1 KNO3溶液25mL,恰好反应完全。该反应的方程式为:
FeSO4 +KNO3 +H2SO4→K2SO4 +Fe2(SO4)3+NxOy + H2O(未配平),则对该反应的下列说法正确的是 A.化学方程式中按物质顺序的计量数是:8、2、5、1、4、1、5B.反应中氧化产物是N2OC.反应过程中转移的电子数为8mol电子D.氧化产物和还原产物的物质的量之比为4∶1
题型:未知 难度:其他题型
答案
AD
解析
该反应中,Fe2+失电子Fe3+,所以硫酸亚铁作还原剂;硝酸钾中氮元素得电子化合价降低作氧化剂;硫酸亚铁的物质的量0.1mol,所以硫酸亚铁生成硫酸铁失去0.1mol电子;根据氧化还原反应中得失电子数相等可知,硝酸钾中氮元素得到0.1mol电子,KNO3物质的量为0.025mol,则0.025*(5-2Y/X)=0.1即X=2Y,按照A的配平系数带入答案,经过验证,所以该氮的氧化物是N2O,应该是还原产物,A正确,BC错误;氧化产物是Fe2(SO4)3和还原产物N2O的物质的量之比为4∶1,正确;
考点
据考高分专家说,试题“在5.6 g Fe粉中加入过量的稀硫酸溶.....”主要考查你对 [氧化还原反应与基本反应类型的关系 ]考点的理解。
氧化还原反应与基本反应类型的关系
氧化还原反应与基本反应类型的关系:
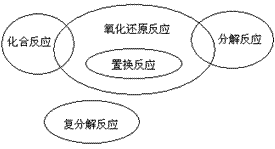
化合反应有单质参加的是氧化还原反应;分解反应有单质生成的是氧化还原反应;置换反应全部是氧化还原反应;复分解反应都是非氧化还原反应
化学反应的分类:
化学反应按照不同的分类标准,可以分成不同的反应类型
- 根据原子(原子团)的组合形式来分类,把化学反应分为化合反应、分解反应、置换反应、复分解反应,
但是四种基本类型的反应并不能包括所有的化学反应,比如3O2==2O3。 - 按是否有电子转移,把化学反应分为氧化还原反应和非氧化还原反应。
- 按是否有离子参加反应,把化学反应分为离子反应和非离子反应。
- 按化学反应的能量关系,把化学反应分为放热反应和吸热反应。
- ……
null
null
null
null
null