题文
甲、乙两同学研究Na2SO3溶液与FeCl3溶液反应的情况。
步骤
操作
现象
I
向2 mL 1 mol·L-1FeCl3溶液中加入一定量的Na2SO3溶液
溶液由棕黄色变为红褐色,
并有少量刺激性气味的气体逸出
(1)常温下,FeCl3溶液的pH_______7(填“<”、“>”或“=”)。
(2)分析红褐色产生的原因。
① 甲同学认为步骤I中溶液呈红褐色是因为生成了Fe(OH)3,用化学平衡移动原理解释溶液呈红褐色的原因:________。
② 乙同学认为可能是发生了氧化还原反应,完成并配平其反应的离子方程式:
Fe3+ +
SO32- +
=
F e2+ +
+

乙同学查阅资料得知:
1.Fe2+与SO32-反应生成墨绿色的絮状沉淀FeSO3;
2.墨绿色的FeSO3与黄色的FeCl3溶液混合后,溶液呈红褐色。
(3)甲同学为了确认溶液呈红褐色的原因是生成了Fe(OH)3,设计并完成了如下实验:
步骤
操作
现象
II
用激光笔照射步骤I中的红褐色溶液
出现“丁达尔效应”
甲同学因此得出结论:溶液呈红褐色是因为生成了Fe(OH)3。而乙同学认为甲同学得出结论的证据仍然不足,乙同学的理由是________。
(4)为进一步确认Na2SO3溶液与FeCl3溶液反应的情况,乙同学设计并完成了如下实验:
步骤
操作
现象
III
向1 mol•L-1的FeCl3溶液中通入一定量的SO2
溶液由黄色变为红褐色
IV
用激光笔照射步骤III中的红褐色溶液
没有出现“丁达尔效应”
① 经检验步骤III中红褐色溶液含有Fe2+,检验Fe2+选用的试剂是_________(填字母)。
a.K3[Fe(CN)6] 溶液 b.KSCN溶液 c.KMnO4溶液
② 已知H2SO3是弱酸,请结合电离方程式说明步骤III中出现红褐色的原因: 。
(5)结论:由上述实验得知,甲、乙两同学所持观点均正确。
题型:未知 难度:其他题型
答案
(1)<(2)①Fe3++3H2O
Fe(OH)3+3H+,加入Na2SO3后,c(H+)下降,平衡正向移动,生成Fe(OH)3②2Fe3+ + SO32- +H2O = 2Fe2+ +SO42-+2H+(3)FeSO3和FeCl3的混合溶液也可能出现“丁达尔效应”(4)①a ②H2SO3
H++HSO3—;HSO3—
H++SO32—,SO32—与被还原生成的Fe2+结合为FeSO3,与剩余的FeCl3溶液混合而呈现红褐色
解析
(1)铁离子在溶液中水解生成Fe(OH)3产生H+,故溶液pH<7;(2)①溶液中铁离子水解生成Fe(OH)3产生红褐色沉淀,Fe3++3H2O
Fe(OH)3+3H+,加入Na2SO3后,SO32-与H+反应生成SO2,使溶液中c(H+)下降,平衡正向移动,促进水解进行②2Fe3++SO32-+H2O = 2Fe2++SO42+2H+②由题意知铁元素的化合价降低,生成亚铁离子,硫元素化合价升高生成硫酸根离子,故反应方程式2Fe3+ + SO32- +H2O = 2Fe2+ +SO42-+2H+(3)由查阅到的资料可知墨绿色的FeSO3与黄色的FeCl3溶液混合后,溶液呈红褐色,也可产生“丁达尔现象”故无法确定是否为Fe(OH)3(4)①亚铁离子和铁氰化钾溶液反应生成蓝色沉淀,这是亚铁离子的特征反应,故a正确 ②H2SO3分步电离生成SO32—,SO32—与被还原生成的Fe2+结合为FeSO3,与剩余的FeCl3溶液混合而呈现红褐色,H2SO3
H++HSO3—,HSO3—
H++SO32—,Fe2+ + SO32- = FeSO3。
考点
据考高分专家说,试题“甲、乙两同学研究Na2SO3溶液与FeC.....”主要考查你对 [氧化还原反应与基本反应类型的关系 ]考点的理解。
氧化还原反应与基本反应类型的关系
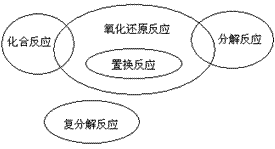
氧化还原反应与基本反应类型的关系:
化合反应有单质参加的是氧化还原反应;分解反应有单质生成的是氧化还原反应;置换反应全部是氧化还原反应;复分解反应都是非氧化还原反应
化学反应的分类:
化学反应按照不同的分类标准,可以分成不同的反应类型
- 根据原子(原子团)的组合形式来分类,把化学反应分为化合反应、分解反应、置换反应、复分解反应,
但是四种基本类型的反应并不能包括所有的化学反应,比如3O2==2O3。 - 按是否有电子转移,把化学反应分为氧化还原反应和非氧化还原反应。
- 按是否有离子参加反应,把化学反应分为离子反应和非离子反应。
- 按化学反应的能量关系,把化学反应分为放热反应和吸热反应。
- ……
null
null
null
null
null