题文
“低碳循环”引起世界各国的高度关注,而如何降低大气中CO2的含量及有效地开发利用CO2,更是引起了全世界的普遍重视。
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请配平该反应的化学方程式:(将化学计量数按顺序填在答题卷上)
___C+____KMnO4+____H2SO4→___CO2↑+____MnSO4+____K2SO4+___H2O
(2)将不同最的CO(g)和H2O(g)分别通人到容积为2L的恒容密闭容器中,进行如下反应:
CO(g)+H2O(g)
CO2(g)+H2(g) 得到表中三组数据
实验
温度℃
起始量/mol
平均量/mol
达到平衡所需时间/min
CO
H2O
H2
CO
1
650
4
2
1.6
2.4
6
2
900
2
1
0.4
1.6
3
3
900
a
b
c
d
t
①实验1中以v (CO2)表示的反应速率为____(取二位小数,下同)。
②实验3条件下,反应物和生成物的起始量、平衡量都不知道,欲计算该条件下的化学平衡常数可以利用实验____的数据进行,其K=____。
(3)已知在常温常压下:
①2CH3OH(I)+3O2(g)=2CO2(g)+4H2O(g) △H=-1275.6kJ/mol
②2CO(g)+O2(g)=2CO(g) △H=-566.0kJ/mol
③H2O(g)=H2O(I) △H=-44.0kJ/mol
写出甲醇(CH2OH)不宪全燃烧生成一氧化碳和液态水的热化学方程式_ 。
题型:未知 难度:其他题型
答案
(12分)(1)5、4、6、5、4、2、6(3分)
(2)①0.13mol/(L•min)(2分);②2(2分);0.17(2分)
(3)CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H=-442.8KJ/mol(3分)
解析
(1)根据反应的化学方程式可知,碳元素化合价由0价升高到+4价,失去4个电子。Mn元素化合价由+7价降低为+2价,得到5个电子,最小公倍数为20,所以C的系数为5,KMnO4系数为4,结合原子守恒配平后方程式为5C+4KMnO4+6H2SO4=5CO2↑+4MnSO4+2K2SO4+6H2O。
(2)①由表中数据可知,6min平衡时H2的物质的量为1.6mol,浓度=1.6mol÷2L=0.8mol/L,所以v(H2)=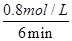
=0.13mol/(L•min)。又因为反应速率之比等于化学计量数之比,故v(CO2)=v(H2)=0.13mol/(L•min)。
②由于平衡常数只与温度有关系,所以欲计算900℃时该反应的平衡常数,则可以利用第2组实验中的数据。平衡时CO的物质的量为1.6mol,则:
CO(g)+H2O(g)
CO2(g)+H2(g)
起始量(mol) 2 1 0 0
转化量(mol) 0.4 0.4 0.4 0.4
平衡量(mol) 1.6 0.6 0.4 0.4
该反应前后气体体积不变,故利用物质的量代替浓度计算平衡常数,所以900℃时该反应平衡常数K=
=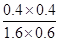
=0.17。
(3)根据盖斯定律可知,①-②+③×4即得到反应2CH3OH(l)+2O2(g)=2CO(g)+4H2O(l),所以该反应的反应热△H=-1275.6kJ/mol+566.0kJ/mol-44.0kJ/mol×4=-885.6KJ/mol,所以该反应的热化学方程式是CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H=-442.8KJ/mol。
考点
据考高分专家说,试题“ “低碳循环”引起世界各国的高度关注,而.....”主要考查你对 [氧化还原反应的配平 ]考点的理解。
氧化还原反应的配平
配平简介:
化学反应方程式严格遵守质量守恒定律,书写化学反应方程式写出反应物和生成物后,往往左右两边各原子数目不相等,不满足质量守恒定律,这就需要通过配平来解决。
配平原则:
(1)电子守恒原则:反应中还原剂失去电子的总数与氧化剂得到电子的总数相等
(2)电荷守恒原则:若为离子反应,反应前后离子所带正负电荷总数相等
(3)质量守恒原则:反应前后各元素的原子个数相等
配平步骤:
(1)一标:标明反应前后化合价有变化的元素的化合价
(2)二等:通过求最小公倍数使化合价升降总值相等
(3)三定:确定氧化剂与还原剂的化学计量数
氧化剂(还原剂)化学计量数=降(升)价的最小公倍数÷1mol氧化剂(还原剂)降(升)价总数
(4)四平:用观察法配平其他物质的化学计量数
(5)五查:检查质量与电荷、电子是否分别守恒
配平技巧:
(1)逆向配平法:部分氧化还原反应、自身氧化还原反应等可用逆向配平法,即选择氧化产物、还原产物为基准物来配平(一般从反应物很难配平时,可选用逆向配平法)
例:
通过表明氧化产物、还原产物化合价的升降,确定CrCl3、Cl2的计量数为2和3,然后再用观察法配平。
(2)设“1”配平法:设某一反应物或生成物(一般选用组成元素较多的物质作基准物)的化学计量数为1,其余各物质的化学计量数可根据原子守恒原理列方程求得。
例:P4O+Cl2→POCl3+P2Cl6
可令P4O前的系数为1,Cl2的系数为x,则
1P4O+xCl2→POCl3+3/2P2Cl6 ,再由Cl原子守恒得2x=3+3/2×6 得x=6 即可配平
(3)零价配平法:先令无法用常规方法确定化合价的物质中各元素均为零价,然后计算出各元素化合价的升降值,并使元素化合价升降总数相等,最后用观察法配平其他物质的化学计量数。
例:Fe3C+HNO3=Fe(NO3)3+CO2↑+NO2↑+H2O
复杂化合物Fe3C按照常规方法分析,无法确定其Fe和C的具体化合价,此时可令组成物质的各元素化合价为零价,根据化合价升降法配平。
通过表明氧化产物、还原产物化合价的升降,确定CrCl3、Cl2的计量数为2和3,然后再用观察法配平。
(2)设“1”配平法:设某一反应物或生成物(一般选用组成元素较多的物质作基准物)的化学计量数为1,其余各物质的化学计量数可根据原子守恒原理列方程求得。
例:P4O+Cl2→POCl3+P2Cl6
可令P4O前的系数为1,Cl2的系数为x,则
1P4O+xCl2→POCl3+3/2P2Cl6 ,再由Cl原子守恒得2x=3+3/2×6 得x=6 即可配平
(3)零价配平法:先令无法用常规方法确定化合价的物质中各元素均为零价,然后计算出各元素化合价的升降值,并使元素化合价升降总数相等,最后用观察法配平其他物质的化学计量数。
例:Fe3C+HNO3=Fe(NO3)3+CO2↑+NO2↑+H2O
复杂化合物Fe3C按照常规方法分析,无法确定其Fe和C的具体化合价,此时可令组成物质的各元素化合价为零价,根据化合价升降法配平。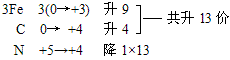
再用观察法确定物质的化学计量数。
(4)整体标价法:当某元素的原子在某化合物中有数个时,可将它作为一个整体对待,根据化合物中元素化合价代数和为零原则予以整体标价。
例:S+Ca(OH)2→CaSx+Ca2S2O3+H2O
生成物CaSx、Ca2S2O3中的Sx、S2作为一个整体标价为-2、+4价,则化合价升降关系为:
Sx 0→-2 降2×2
S2 0→+4 升4×1
即可配平。
(5)缺项配平法:一般先确定氧化剂、还原剂、氧化产物、还原产物的化学计量系数,再通过比较反应物与生成物,确定缺项(一般为H2O、H+或OH-),最后观察配平。
(6)有机氧化还原反应的配平:有机物中元素的化合价一般来讲,氢元素显+1价,氧元素显-2价,然后再根据化合价的代数和为零求酸碳元素的平均化合价。
氧化还原反应方程式配平的一般方法与步骤:
- 一般方法:从左向右配。
- 步骤:标变价,找变化,求总数,配系数。
- 标出元素化合价变化的始态和终态
- 求升价元素或降价元素化合价的变化数
- 求化合价变化数的最小公倍数,分别作为氧化剂或还原剂的系数
- 配平变价元素
- 用观察法配平其他元素
- 检查配平后的方程式是否符合质量守恒定律(离子方程式还要看电荷是否守恒)
如: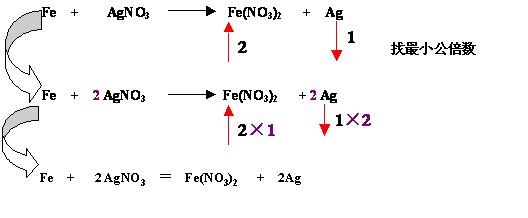
特殊技巧:
配平时若同一物质内既有元素的化合价上升又有元素的化合价下降,若从左向右配平较困难,可以采用从右向左配平,成为逆向配平法。
null
null
null
null
null
null
null
null




