题文
(14分)X、Y、Z、W、P为短周期的主族元素,其原子序数依次增大。Y、Z、W、P位于同一周期。X 元素形成的单质是自然界中含量最多的气体,1mol Y的单质分别与足量盐酸和氢氧化钠溶液反应生成的气体在标况下均为33.6L。W的原子最外层电子数与核外电子总数之比为3:8,X的原子序数是Z的原子序数的一半。
(1)Y在周期表中的位置是________;X的氢化物与P的氢化物接近时的现象是_________。
(2)W与P可形成原子个数比为1:2的化合物,其电子式为__________。
(3)Y与P形成的化合物溶液显____性;用离子反应方程式表示显这种性质的原因________________。
(4)Z、W、P三种元素的气态氢化物稳定性由高到低的顺序是______________________(填化学式)。
(5)X的三氟化物是微电子工业中优良的等离子刻蚀气体,但在潮湿的环境中能与水发生反应生成无色气体,遇空气变为红棕色。写出此三氟化物与水反应的化学反应方程式_____,若0.6mol X的三氟化物完全与水反应,则转移的电子总数约为_________个。
题型:未知 难度:其他题型
答案
(1)第三周期第ⅢA族;产生大量白烟 (2)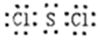
(3)酸;Al3++3H2O
Al(OH)3+3H+ (4)HCl H2S SiH4
(5)3NF3+5H2O═2NO↑+HNO3+9HF;2.408×1023
解析
X、Y、Z、W、P为短周期的主族元素,其原子序数依次增大,Y、Z、W、P位于同一周期,X元素形成的单质是自然界中含量最多的气体,则X是N元素;1mol Y的单质分别与足量盐酸和氢氧化钠溶液反应生成的气体在标况下均为33.6L,能和盐酸、氢氧化钠溶液反应且放出气体的物质只有Al,所以Y是Al元素;W的原子最外层电子数与核外电子总数之比为3:8,W的原子序数大于13,且为短周期元素,所以其最外层电子数与其核外电子总数分别是6、16,则W是S元素;X的原子序数是Z的原子序数的一半,所以Z是Si元素,P为短周期主族元素,且原子序数大于16,所以P是Cl元素。
(1)铝元素的原子序数是16,在周期表中的位置是第三周期第ⅢA族;氨气与氯化氢混合迅速反应生成氯化铵,产生大量白烟。
(2)S与Cl可形成原子个数比为1:2的化合物为SCl2,每个氯原子形成1个共用电子对、硫原子形成2个共用电子对,所以其电子式为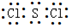
。
(3)Y与P形成的化合物是氯化铝,其溶液显酸性,是由于铝离子水解导致的,离子方程式为Al3++3H2O
Al(OH)3+3H+。
(4)元素非金属性越强,其氢化物越稳定,同一周期元素中,元素的非金属性随着原子序数的增大而增强,所以其氢化物越稳定,因此Si、S、Cl三种元素的气态氢化物稳定性由高到低的顺序是 HCl>H2S>SiH4。
(5)NCl3在潮湿的环境中能与水发生反应生成无色气体,遇空气变为红棕色,说明生成NO,同时还生成硝酸和氢氟酸,该反应的化学方程式为3NF3+5H2O═2NO↑+HNO3+9HF,根据NCl3与转移电子之间的关系式得,转移电子数=
×1×(5−3)NA/mol=2.408×1023。
考点
据考高分专家说,试题“(14分)X、Y、Z、W、P为短周期的主.....”主要考查你对 [氧化还原反应的配平 ]考点的理解。
氧化还原反应的配平
配平简介:
化学反应方程式严格遵守质量守恒定律,书写化学反应方程式写出反应物和生成物后,往往左右两边各原子数目不相等,不满足质量守恒定律,这就需要通过配平来解决。
配平原则:
(1)电子守恒原则:反应中还原剂失去电子的总数与氧化剂得到电子的总数相等
(2)电荷守恒原则:若为离子反应,反应前后离子所带正负电荷总数相等
(3)质量守恒原则:反应前后各元素的原子个数相等
配平步骤:
(1)一标:标明反应前后化合价有变化的元素的化合价
(2)二等:通过求最小公倍数使化合价升降总值相等
(3)三定:确定氧化剂与还原剂的化学计量数
氧化剂(还原剂)化学计量数=降(升)价的最小公倍数÷1mol氧化剂(还原剂)降(升)价总数
(4)四平:用观察法配平其他物质的化学计量数
(5)五查:检查质量与电荷、电子是否分别守恒
配平技巧:
(1)逆向配平法:部分氧化还原反应、自身氧化还原反应等可用逆向配平法,即选择氧化产物、还原产物为基准物来配平(一般从反应物很难配平时,可选用逆向配平法)
例:
通过表明氧化产物、还原产物化合价的升降,确定CrCl3、Cl2的计量数为2和3,然后再用观察法配平。
(2)设“1”配平法:设某一反应物或生成物(一般选用组成元素较多的物质作基准物)的化学计量数为1,其余各物质的化学计量数可根据原子守恒原理列方程求得。
例:P4O+Cl2→POCl3+P2Cl6
可令P4O前的系数为1,Cl2的系数为x,则
1P4O+xCl2→POCl3+3/2P2Cl6 ,再由Cl原子守恒得2x=3+3/2×6 得x=6 即可配平
(3)零价配平法:先令无法用常规方法确定化合价的物质中各元素均为零价,然后计算出各元素化合价的升降值,并使元素化合价升降总数相等,最后用观察法配平其他物质的化学计量数。
例:Fe3C+HNO3=Fe(NO3)3+CO2↑+NO2↑+H2O
复杂化合物Fe3C按照常规方法分析,无法确定其Fe和C的具体化合价,此时可令组成物质的各元素化合价为零价,根据化合价升降法配平。
通过表明氧化产物、还原产物化合价的升降,确定CrCl3、Cl2的计量数为2和3,然后再用观察法配平。
(2)设“1”配平法:设某一反应物或生成物(一般选用组成元素较多的物质作基准物)的化学计量数为1,其余各物质的化学计量数可根据原子守恒原理列方程求得。
例:P4O+Cl2→POCl3+P2Cl6
可令P4O前的系数为1,Cl2的系数为x,则
1P4O+xCl2→POCl3+3/2P2Cl6 ,再由Cl原子守恒得2x=3+3/2×6 得x=6 即可配平
(3)零价配平法:先令无法用常规方法确定化合价的物质中各元素均为零价,然后计算出各元素化合价的升降值,并使元素化合价升降总数相等,最后用观察法配平其他物质的化学计量数。
例:Fe3C+HNO3=Fe(NO3)3+CO2↑+NO2↑+H2O
复杂化合物Fe3C按照常规方法分析,无法确定其Fe和C的具体化合价,此时可令组成物质的各元素化合价为零价,根据化合价升降法配平。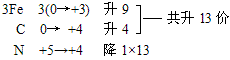
再用观察法确定物质的化学计量数。
(4)整体标价法:当某元素的原子在某化合物中有数个时,可将它作为一个整体对待,根据化合物中元素化合价代数和为零原则予以整体标价。
例:S+Ca(OH)2→CaSx+Ca2S2O3+H2O
生成物CaSx、Ca2S2O3中的Sx、S2作为一个整体标价为-2、+4价,则化合价升降关系为:
Sx 0→-2 降2×2
S2 0→+4 升4×1
即可配平。
(5)缺项配平法:一般先确定氧化剂、还原剂、氧化产物、还原产物的化学计量系数,再通过比较反应物与生成物,确定缺项(一般为H2O、H+或OH-),最后观察配平。
(6)有机氧化还原反应的配平:有机物中元素的化合价一般来讲,氢元素显+1价,氧元素显-2价,然后再根据化合价的代数和为零求酸碳元素的平均化合价。
氧化还原反应方程式配平的一般方法与步骤:
- 一般方法:从左向右配。
- 步骤:标变价,找变化,求总数,配系数。
- 标出元素化合价变化的始态和终态
- 求升价元素或降价元素化合价的变化数
- 求化合价变化数的最小公倍数,分别作为氧化剂或还原剂的系数
- 配平变价元素
- 用观察法配平其他元素
- 检查配平后的方程式是否符合质量守恒定律(离子方程式还要看电荷是否守恒)
如: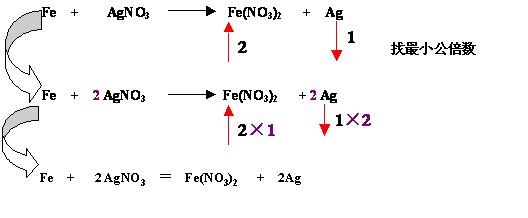
特殊技巧:
配平时若同一物质内既有元素的化合价上升又有元素的化合价下降,若从左向右配平较困难,可以采用从右向左配平,成为逆向配平法。
null
null
null
null
null
null
null
null




