电子的发现
汤姆孙研究阴极射线发现了电子,从而敲开了人类认识原子的大门.
1. 阴极射线:在研究气体导电的玻璃管内有阴、阳两极,若在两极间加一定电压,阴极便发出一种射线,这种射线称为阴极射线。
结论:阴极射线中粒子所带电荷为负电荷。
4.带电粒子比荷 e/m 的推导过程
偏转角 θ 与电场强度 E、极板长度 L 以及带电粒子的速度 v 的关系为
(1)电子的电荷量为 e = 1.602176634×10-19 C。电子电荷量e 为最小的电荷量,称为元电荷。电子质量 m= 9.10938356×10-31 kg,质子质量是电子质量的 1836 倍。
(2)任何带电体的电荷只能是元电荷 e 的整数倍。
7. 发现电子的意义
(1)电子是原子的基本组成部分。
(2)原子还可以再分,除了电子,还包括质量较大且带正电的粒子。
原子的核式结构模型
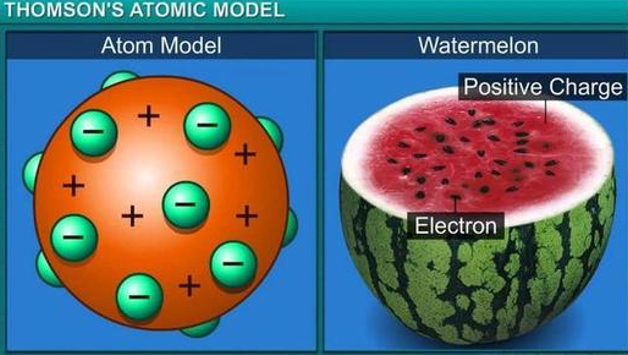
1. 汤姆孙的“枣糕”模型
“枣糕”模型:原子是个球体,正电荷弥漫性地均匀分布在整个球体内,电子镶嵌其中。 缺陷:不能解释高速电子穿透原子及电子发生大角度偏转的现象。
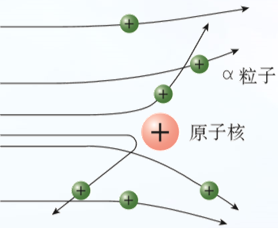
2. α 粒子散射实验
汤姆孙枣糕模型的理论预测:由于正电荷的均匀分布,那么α粒子通过原子时,粒子两侧的正电荷对它的库仑斥力大部分相互抵消,α粒子运动的影响不会很大。
实验探究:在真空中,一束 α 粒子打在金箔上,通过探测屏或者放大镜观察某一时间内向某一方向散射的 α 粒子数。
①在原子的中心有一个很小的核,叫做原子核。
②原子的全部正电荷和几乎全部质量都集中在原子核里。
③带负电的电子在核外空间绕着核旋转。
原子核的电荷与尺度
1. 原子核的电荷: 原子核的电荷数等于核外电子数,等于原子序数。
2. 原子核的尺度: 原子核大小的数量级为10-15 m,原子大小数量级为10-10 m,两者相差十万倍之多,可见原子内部十分“空旷”。若原子相当于一个立体的足球场的话,则原子核就象足球场中的一粒米。