题文
有A、B、C、D、E五种短周期元素,且相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的氢氧化物是两性氢氧化物, E的阳离子与A的阴离子核外电子层结构相同。
解析
设A的原子序数是x,则根据元素在周期表中的相对位置可知,BCD的原子序数分别是x+7、x+8、x+9,所以x+x+7+x+8+x+9=56,解得x=8,则A好似氧元素,B是P元素,C是S元素,D是氯元素。E的氢氧化物是两性氢氧化物,所以E是Al元素。
(1)B元素在周期表中的位置为第三周期ⅤA族。
(2)A与氢元素能形成原子物质的量之比为1∶1的化合物是双氧水,含有极性键和非极性键,其电子式是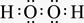
。
(3)由于H2O分子之间存在氢键,所以水的沸点高于H2S的沸点。
(4)同周期自左向右,原子半径逐渐减小,则、C、D的原子半径由大到小的顺序为P > S > Cl。
(5)铝是活泼的金属,石墨是能导电的非金属,则①中铝是负极,总的反应式是2Al + 6H+ = 2Al3++ 3H2↑;由于铝也能和氢氧化钠溶液反应,所以②中也能构成原电池,其中铝是负极,总的反应式是2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和应试能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力,考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。
考点
据考高分专家说,试题“有A、B、C、D、E五种短周期元素,且相.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




